Elektrontransportkjeden er lokalisert i den indre mitokondriemembranen hvor elektroner fra NADH blir overført til oksygen i elektrontransportkjeden. NADH må også oksideres videre for at det ikke skal bli mangel på NAD+ i mitokondriene. Hos bakterier finnes elektrontransportkjeden i plasmamembranen.
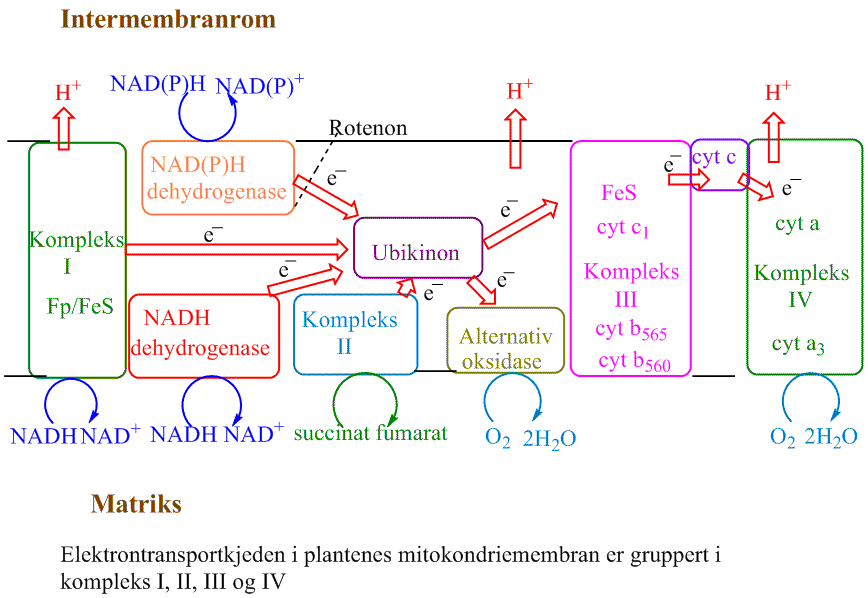
Elektrontransportkjeden i mitokondriene består av 4 proteinkomplekser (I-IV).
I kompleks I som inneholder FMN (flavomononukleotid) i flavoproteiner, smat jernsvovelproteiner, overføres elektroner fra NADH + H+ til kinonet ubikinon katalysert av av enymzet NADH dehydrogenase. I kompleks I blir protoner (H+) til intermembranrommet mellom ytre og indre mitokondriemembran (cristae).
Succinat blir oksidert i kompleks II av membranbundet succinat dehydrogenase fra sitronsyresyklus. Elektroner fra succinat overføres via FADH2 og jernsvovelprotiner til ubikinon. Elektroner fra kompleks I, II og NADPH blir overført til ubikinon, men det kommer ikke bidrag til protongradienten fra kompleks II.
I kompleks III, som virker som en ubikinol-cytokrom c oksidoreduktase, overføres elektroner til cytokrom c og det dannes 4 H+ per elektron som fraktes inn i intermembranrommet.
Kompleks IV er den terminale cytokrom c oksidase hvor ett oksygenmolekyl reduseres til 2 vannmolekyler ved å motta 4 elektroner.
Til forskjell fra dyr har planter en NAD(P)H dehydrogenase festet til mitokondriemembranen mot intermembranrommet, og som kan levere elektroner til ubikinon.
Elektrontransportkjeden er koblet til protontransport ut i mellomrommet mellom de to mitokondriemembranene, og den protondrivende kraften dette gir.
ADP:O forholdet angir forholdet mellom antall ATP som lages når 2 elektroner overføres til et oksygenatom. Ut fra dette forholdet antar man et det lages kjemiosmotisk ATP ved oksidativ fosforylering i kompleks I, III og IV. Den indre mitokondriemembranen er ikke permeabel for H+ slik at det kan bygge seg opp en protonelektrokjemisk gradient over membranen.
ATP syntase
Protongradienten kobles til ATP syntese via enzymkomplekset F0F1 ATP syntase (ATP syntase). Den hydrofobe F0 delen av proteinet er en integrert del av membranen og lager en protonkanal. Når protoner passerer kanalen skjer katalyttisk dannelse av ATP fra ADP og Pi i den hydrofile roterende delen F1. F1 består av 5 forskjellige proteinsubenheter. g-subenheten sitter som et roterende skaft omgitt av a, b, d og e-subenheter med 3 katalyttiske seter i åpen, løs og tett proteinkonformasjon. Substratene ADP og Pi kan binde seg det åpne sete og ATP frigis i fra det tette konformasjonssete.
Avkoblere
Avkoblere blokkerer kobling mellom elektrontransport i elektrontransportkjeden i mitokondriene og fosforylering. Protongradienten kollapser. Mitchells kjemiosmotiske hypotese for ATP syntese forklarer virkningsmekanismen for avkoblere. Derved hemmes syntesen av ATP uten å blokkere elektrontransporten. Det finnes både uorganiske og organiske avkoblere, slik som avkoblerproteiner. Avkoblerproteiner finnes i den indre mitokondriemembranen, og hos pattedyr kjenner man til fem forskjellige avkoblerproteiner, hvorav en av dem kalles termogenin. Ved å dissipere og fjerne protongradienten ved å virke som en alternativ protonkanal, blir elektrontransporten brukt til å produsere varme i stedet for ATP. Uorganiske avkoblere er fettløselige ionoforer f.eks. 2,4-dinitrofenol er en livsfarlig syntetisk avkobler som har blitt brukt i slankepiller.
Avkoblere gjør membranen permeabel for protoner (H+) og hemmer ATP syntesen, men elektrontransporten kan bli stimulert. Flere avkoblere er stoffer fra sekundærmetabolismen hos sopp og bakterier.
Den protondrivende kraften PMF blir en kombinasjon av elektrokjemisk gradient (Δψ) og pH-gradient:
\(\text{Protondrivende kraft}=\Delta \psi- \frac{2.3\; RT}{F} \Delta pH\)
hvor R er den universelle gasskonstanten, F er Faradays konstant, T er absolutt temperatur.
Tilgangen på ADP og Pi er en viktig reguleringsfaktor for hastigheten på respirasjonen.
ATP syntase kan virke motsatt vei som en protonpumpe (H+-ATPase) drevet av hydrolyse av ATP.
Mitokondrielle avkoblerproteiner
Avkoblerproteiner befinner seg på den indre mitokondriemembranen og fjerne protongradienten ved dissipering. Derved blir protongradienten ikke brukt til å produsere varme, men energigen blir i stedet omsatt til varme. Avkoblerproteinene tilhører en familie mitokondrielle anionbærer proteiner. Disse overfører anioner fra fra hulrommet mellom ytre og indre mitokondremembranen, og H+ i hulrommet mellom membranene blir fraktet inn i stroma. Resultatet blir en protonlekkasje, varmeproduksjon og et redusert membranpotensial i mitokondriene.
Planter inneholder et avkoblerprotein som henter elektroner direkte fra ubikinon i en alternativ cyanid-tolerant oksidase, som gir varmeproduksjon i blomster ved termogenese hvor plantehormonet salicylsyre deltar i signalveien.
Brunt fettvev og termogenese (varmeproduksjon)
Fettcellene (adipocyttene) i brunt fettvev har flere og mindre fettdråper per celle, og de er avlange til forskjell fettdråpene fra i hvitt fettvev. Brunt fettvev har flere mitokondrier med cytokromer enn vanlig fettvev, og cytokromene gir brunrød farge. Ved nedbrytning av fettdråpene fettsyrene fraktet til mitokondriene hvor de via beta-oksidasjon og sitronsyresyklus blir omdannet til CO2 og reduksjonskraft med elektron- og protonkildene NADH og FADH2. I brunt fettvev blir elektrontransporten som genererer protongradienten dissipert i form av varme via en alternativ oksidase. lHos pattedyr kjenner man til fem slike avkoblerproteiner (UCP1-5, "uncoupling protein"). UCP1 blir kalt termogenin og brukes til å produsere varme. UCP2 deltar i regulering av mengden reaktive oksygenforbindelser i mitokondriene. Termogenin gir varmeproduksjon i brunt fettvev og ved muskelskjelving. Istedet for å produsere ATP i oksidasjonen blir det produsert varme ved at protonene kommer tilbake til matriks uten å gå igjennom ATP-syntasekomplekset. Brunt fettvev har som navnet sier brunrød farge som skyldes mange mitokondrier i cellene med rødfarget cytokrom. Dyr med ekte vintersøvn eller vinterdvale (hibernering) slik som hos piggsvin, bjørkemus, hoggorm og flaggermus har brunt fettvev (dyr om vinteren). Nyfødte pattedyr har brunt fettvev, og man antar at det også kan finnes hos voksne. Bjørn og grevling har uekte vintersøvn. Man antar at også noen mennesker har brunt fettvev, hvor maten brukes til å produsere varme istedet for ATP.