Nettsider med emneord «kjemi» - Side 3

Vi inviterer til et seminar for alle som er interesserte i kjemiundervisning. Anledningen er at Truls Grønneberg som har vært leder for skolelaboratoriet i mer enn 30 år, fyller 70 år.

Vi demonstrerer prisippet om at "likt løser likt" ved å prøve ut både polart og upolart stoff i ulike løsemidler. Også vannets polare egenskaper og hydrogenbinding blir demonstrert og diskutert.(Tid 4:21)

Noen av de vanligste legeringene blir vist, og noen av deres egenskaper blir demonstrert. (Tid 4:07)

Manganioner finnes med flere ulike oksidasjonstall og har da forskjellige farger. Dette demonstreres ved å redusere permanganationer i forskjellig grad.(Tid 1:27)

Fordi molekyler og atomer er for små til å kunne observeres, er kjemien helt avhengig av modeller for å forklare det som skjer med stoffene på mikronivå. De vanligste modellene, som blir brukt i kjemiundervisningen, blir vist og drøftet.. (Tid 11:28)

Kjemiske reaksjoner studeres på makronivå, forklares på mikronivå og beskrives med symboler. (Tid 1:17)

Vi ser hvordan man går frem i praksis for å studer fett, proteiner og karbohydrater i noen matvarer. (Tid 7:07)

Vi ser behandling av det meget reaktive metallet natrium, og hvordan det reagerer med vann og med klorgass. (Tid 1:57)

Å brenne metallet magnesium i luft er trivielt, men det at magnesium også brenner friskt i karbondioksid, er mer interessant. (Tid 2:15)
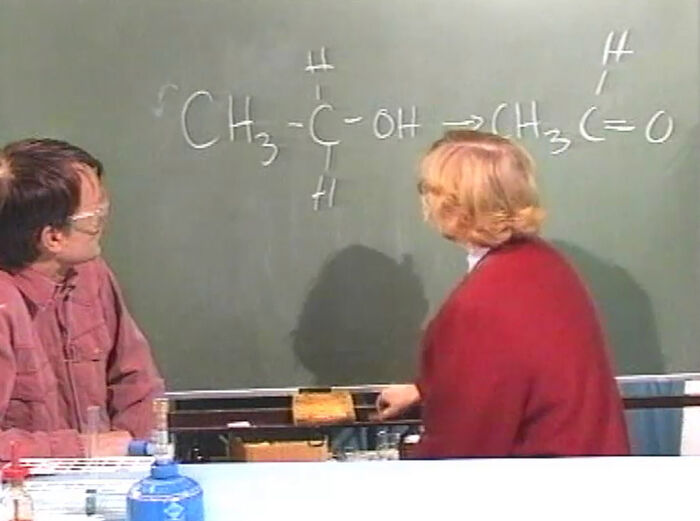
En primær alkohol som etanol påvises ved at den kan oksideres til et aldehyd (her etanal) av kromsyre. Det er denne oksidasjonsreaksjonen som demonstreres og drøftes. (Tid 2:00)

Egenskaper til de vanligste gassene nitrogen, oksygen, hydrogen og karbondioksid gjennomgås og demonstreres. (Tid 9:31)

Vi er vant med at is flyter. Men hva skjer om isbiten har større tetthet enn væsken vi putter den i? (Tid 2:51)
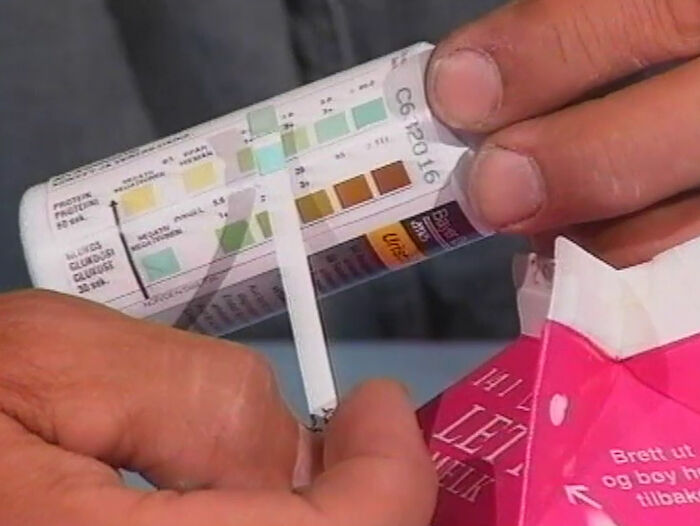
Vi ser enkle påvisningsreaksjoner på glukose, proteiner og stivelse i noen næringsmidler. Reagenser til å påvise slike næringsstoffer kan man vanligvis finne på et apotek. (Tid 2:59)

Vi ser noen store, vakre, dyrkete krystaller, og deretter blir salters egenskaper som ioneforbindelser demonstrert og drøftet. (Tid 6:24)

Å lære elever om betingelsene for forbrenning og brann er en viktig del av naturfaget. Vi må ha noe som kan brenne, oksygen, og høy nok temperatur. Da brenner det. (Tid 9:03)

Vi ser på innhold, bruk og merking av en del hverdagskjemikalier slik de så ut i 1996. (Tid 3:06)

Vi ser bruk og behandling av en del gassbrennere, både for laboratoriet og i hverdagen. (Tid 5:51)

Den energien som avgis eller tas opp i en kjemisk reaksjon, kaller vi kjemisk energi.(Tid 2:29)

Ioneforbindelser (salter) vil være mer eller mindre løselig i vann. Hvis man har to løsninger av lett løselige ioneforbindelser og blander disse, kan man få en felling hvis de nye kombinasjonene av ioner i blandingen gir et tungt løselig salt. (Tid 0:40)

Et enkelt oppsett for å demonstrere elektrolyse, med to grafittelektroder i en løsning av kaliumjodid som er tilsatt litt fenolftalein indikator. (Tid 1:16)
I D/L-systemet for monosakkarider benyttes Fischers projeksjoner. Da tegnes karbonkjeden vertikalt med den mest oksiderte gruppen så høyt oppe som mulig og den mest reduserte gruppen så langt nede som mulig. Nummereringen starter øverst. Horisontale linjer viser grupper som i projiseringen blir liggende over papirplanet mens vertikale linjer viser grupper som ligger under papirplanet. Hvis -OH gruppen på det nederste kirale C-atomet ligger til høyre, hører monosakkaridet til D-serien. Ligger denne -OH-gruppen til venstre, hører det til L-serien.
NB: D/L-systemet sier ikke hvordan monosakkaridet dreier det planpolariserte lyset. Dette blir angitt med (+) for til høyre og (-) for til venstre.
(E. Fischer (1852-1919) professor i organisk kjemi ved Universitetet i Berlin. D fra dexter (lat.) = høyre og laevus (lat.) = venstre.)

