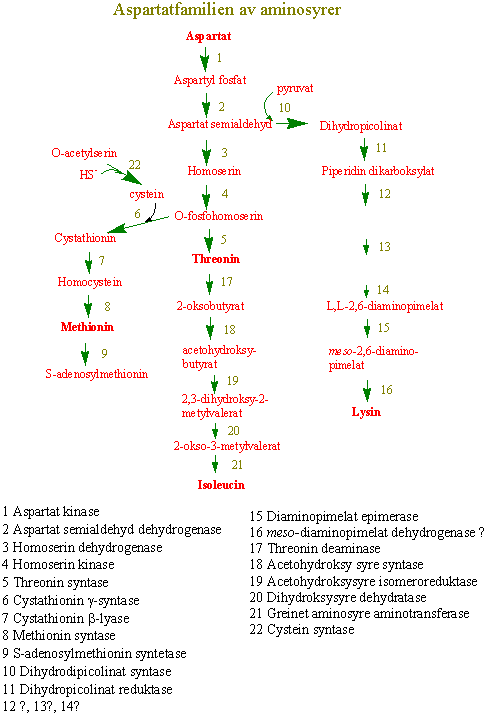
Det er en rekke forskjellige biosynteseveier for aminosyrene i planter, og en del av dem utgjør aminosyrefamilier:

Følgende figurer viser biosynteseveien for aspartatfamilien:
. Doktorgradsarbeidet til undertegnede omfattet rensing og isolering av sentrale enzymer i denne biosynteseveien og studier av deres reguleringsegenskaper og enzymkinetikk i spirende bygg og erter. Frø inneholder protein som en del av opplagsnæringen, og som blir omsatt under frøspiringen. Erter akkumulerer store mengder av aminosyren homoserin under frøspringen. Frøplantene ble knust i en Waring-blender i en bufferløsning som bl.a. inneholdt merkaptoetanol for å beskytte SH-gruppene mot oksidasjon og glycerol for bedre å tåle nedfrysing. Emzymekstraktet bl silt gjennom gaz og deretter sentrifugert i en Sorvall kjølesentrifuge. Alle arbeidsprosessene skjedde i et kjølelaboratorium ved ca. 3-5oC i 2.etasje i Biologibygningen på Blindern, og løsningene ble holdt kaldt på is. Rensingen av enzymene skjedde ved ammoniumsulfatutfelling, gelelektroforese gjennom søyler med forskjellig Sephadex gelmateriale som skiller på størrelsen til proteinene (G-25, G-100, G-200), og ved ionebytting, og samlet opp i en fraksjonssamler Enzymene hadde lav enzymaktivitet og flere av dem ble påvist ved å bruke 14C-merkete aminosyrer som enzymsubstrat. Det radioaktive produktet i enzymreaksjonen ble isolert med høyspent papirkromatografering eller vanlig papirkromatografering, klippet ut, puttet i scinillasjonsglass med scintillasjonsvæske og telt i en Phillips scintillasjonsteller. Noen av subratene i synteseveien var ikke kommersielt tilgjengelig, bl.a. 14C-merket fosfohomosering som jeg laget ved å isolere enzymet homoserin kinase ved autolyse av store mengder bakegjær. Radioaktivt merket fosfohomoserin ble deretter isolert ved brukt av anion- og kationbyttere (Dowex) og derved hadde jeg et substrat som kunne brukes til å studere enzymet threonin syntase. Aspartat semialdehyd var det også umulig å få kjøpt, men ble laget ved ozonolyse av allyl-glycin. Professor Per Kolsaker ved Kjemisk institutt, UiO hadde utstyr for å lage ozon som ble boblet gjennom løsningen, og aspartat semialdehyd ble deretter renset. Derved ble det mulig å studere egenskapene til enzymet homoserin dehydrogenase ved å måle oksidasjonen av NADPH i et spektrofotometer ved 340 nanometer. Det viste seg å være flere isoenzymer, og aspartat kinase er et allosterisk enzym. For å kunne studere denne allosteriske enzymkinetikken fikk jeg tak i et Fortran-program som jeg tilpasset kjøring på UiOs datamaskin, og kunne derved beregne Hill-koeffisienter. Biosyntesen av aminosyren methionin er også interessant for den kan bli omdannet til S-adenosylmethionin som er en viktig metyl-donor i metabolismen, inkludert epigenetikk, og kan også gi opphav til metylmethionin.
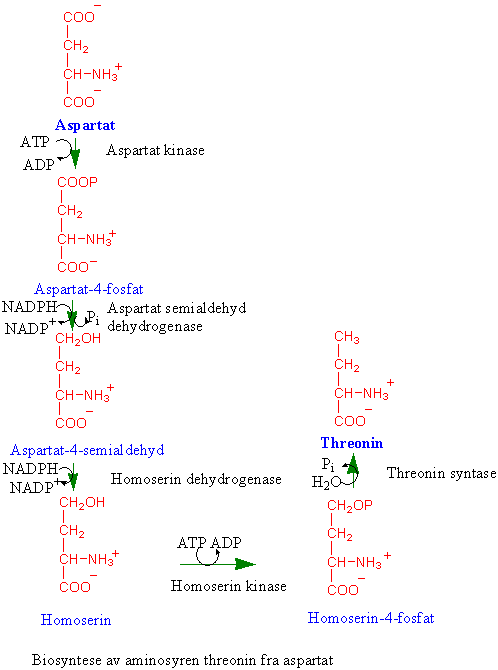
Biosyntese av threonin fra aspartat
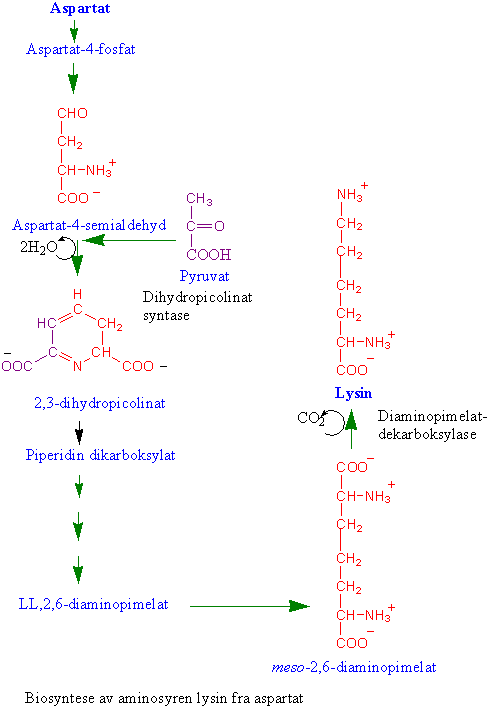
Biosyntesen av aminosyren lysin fra aspartat
Regulering av enzymer i aspartatfamilien ved tilbakekobling
Aspartatfamilien er som alle greinete biosynteseveier sterkt regulert med positive og negative tilbakekoblinger fra endeproduktene.

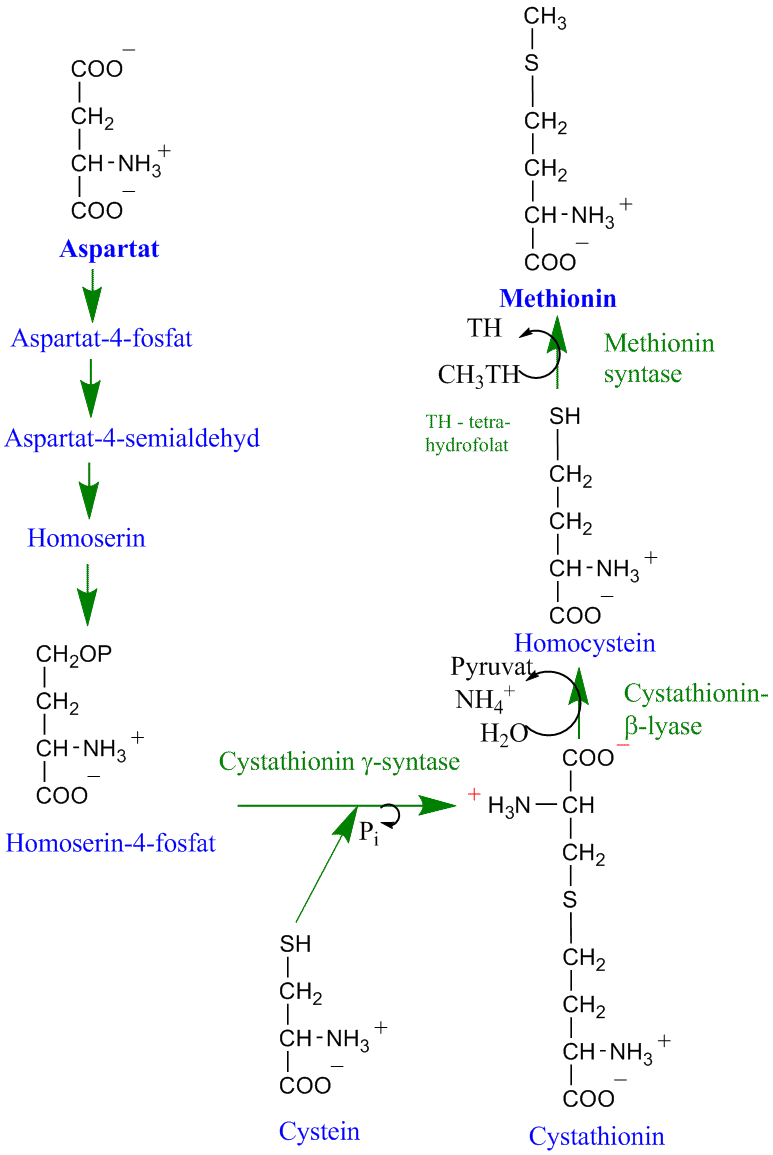
Biosynteseveien fra aspartat til svoelaminosyren metionin
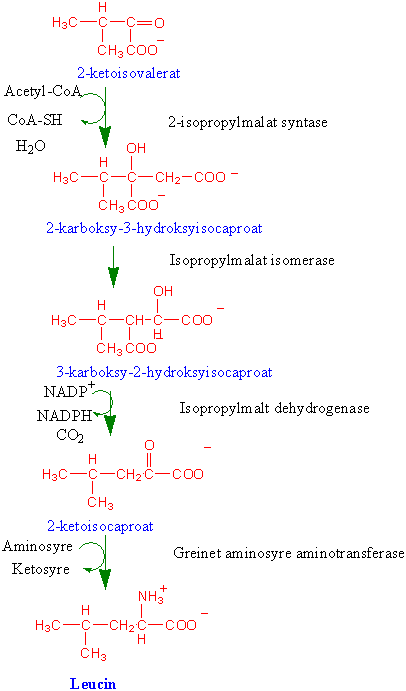
Fra aspartat til de greinete aminosyrene isoleucin, valin og leucin
Biosynteseveien er også utgangspunkt for de greinete aminosyrene isoleucin, valin og leucin: