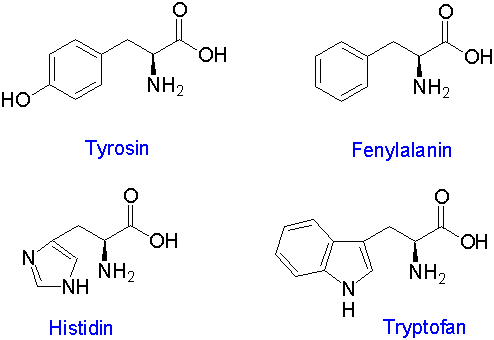
Tyrosin
Tyrosin (l. tyros – ost) ble isolert fra melke- og fosfoproteinet kasein i ost, gjort av den tyske kjemikeren Justus von Liebig. I planter og bakterier blir tyrosin laget fra prefenat, et intermediat i shikimatveien. Prefenat blir oksidativt dekarboksylert.
Tyrosin deltar i :
- Signalveier via reseptor tyrosin kinase hvor fosforylering av hydroksylgruppen endrer signalaktiviteten til proteinet.
- I fotosystem II i fotosystem II er det et spesielt tyrosin i proteiner som virker som elektrondonor i reduksjonen av oksidert klorofyll. Deprotonering av hydroksylgruppen gir et tyrosin-radikal som blir redusert via fire manganmolekyler i en klynge.
- I lateksen fra opiumsvalmuen (Papaver somniferum) blir tyrosin brukt som utgangsmateriale i biosyntesen av alkaloidet morfin.
I dyr blir fenylalanin og tyrosin brukt til å lage biogene aminer som tyramin, L-DOPA, dopamin, synefrin, epinefrin (adrenalin), norepinefrin (noradrenalin). Tyrosin er også en forkomponent i syntesen av ubikinon og pigmentet melanin.
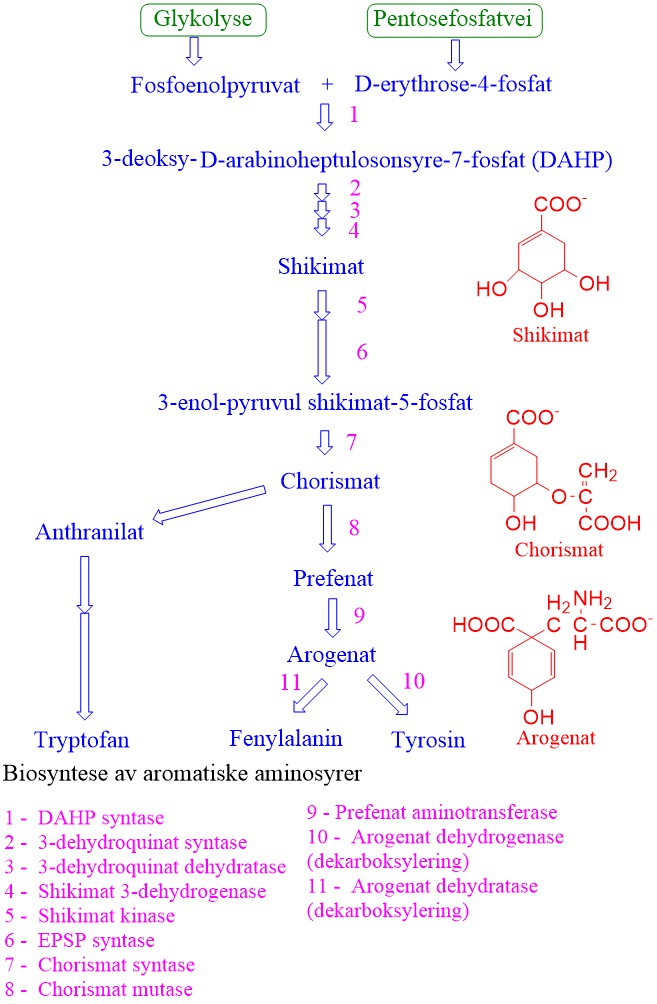
Biosyntese av aromatiske aminosyrer i planter.
Fenylalanin
Fenylalanin har en hydrofob upolar benzylsidekjede. En av proteinaminosyrene. Første gang isolert i 1881 fra frøplanter av gule lupiner (Lupinus luteus). I planter fungerer fenylalanin som forkomponent for biosyntese av flavonoider og lignin.
Fenylalanin er en essensiell aminosyre som vi må ha tilført via maten vi spiser. Hemoglobin har høyt innehold av fenylalanin. Fenylketonuria (Föllings sykdom) skyldes en mangel ved metabolismen slik at kroppen ikke kan omsette fenylalanin. Aspartam(Nutrasweet) er et kunstig søtningsstoff bestående av et dipeptid metylester mellom aminosyrerene aspartat og fenylalanin.
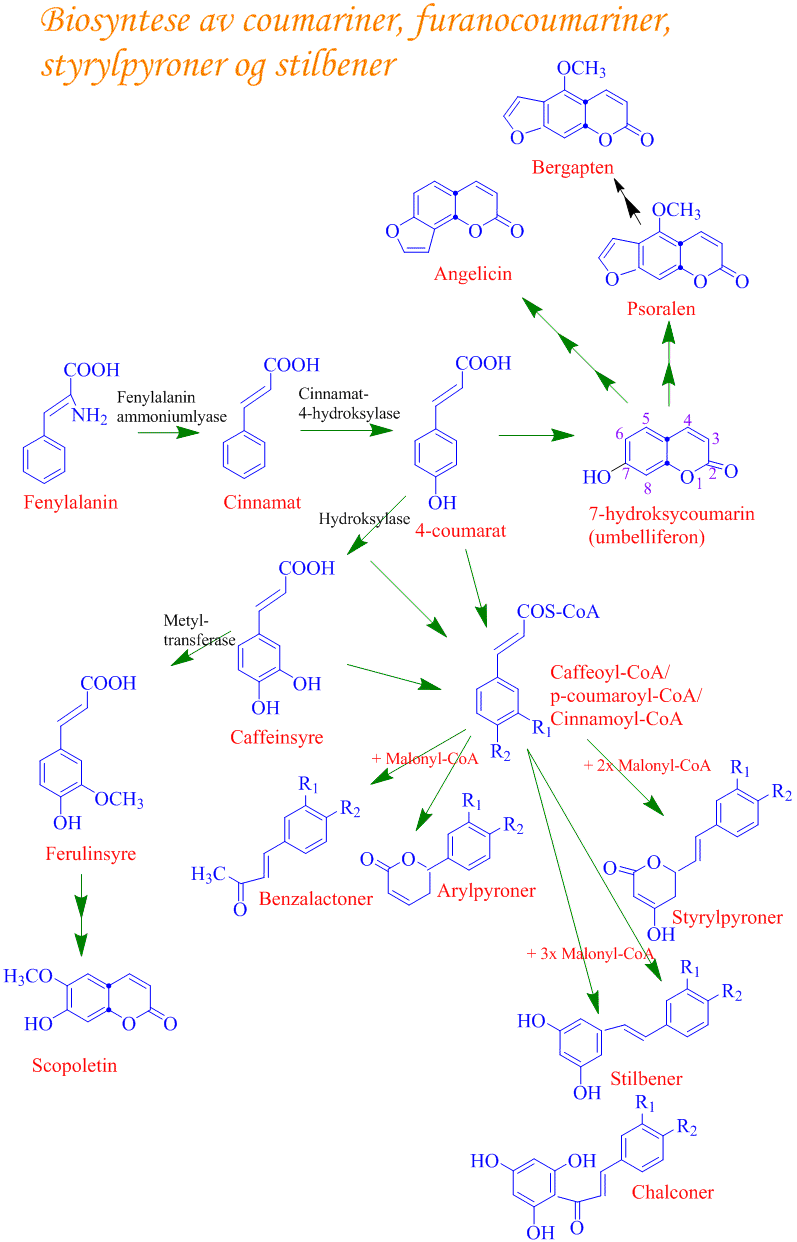
Fenylalanin er utgangsmateriale for biosyntese av en rekke sekundærmetabolitter i planter
Tryptofan
Tryptofan er en essensiell proteinaminosyre som inneholder en indolgruppe. Tryptofan ble første gang isolert i 1901 fra hydrolyse av kasein. Planter og bakterier lager tryptofan fra shikimat eller anthranilat. Plantehormonet auxin blir laget fra tryptofan.
Hos dyr er tryptofan en forkomponent fra naurotransmittoren serotonin, samt søvnhormonet melatonin .
Histidin
Histidin er en essensiell proteinaminosyre med en imidazol-gruppe. Imidiazol kan finnes i protonisert eller nøytral form og kan inngå i flere typer reaksjoner: \(\pi-\pi\)stabel interkasjoner, protonskyttel (i karbon anhydrase) og H-\(\pi\) interaksjoner eller som koordinerende ligand for toverdige kationer som kalsium (Ca2+) og zink (Zn2+). Histin spiller en viktig i rolle i det aktive sete hos flere enzymer.
Hos dyr kan histidin bli omdannet til histamin katalysert av histidin dekarboksylase. Histamin deltar i en lang rekke fysiologiske reaksjoner i kroppen. Histidin spiller en viktig rolle i stabilisering av oksyhemoglobin.
Shikimatbiosyntesevei og syntese av aromatiske aminosyrer
Shikimatbiosynteseveien finnes i planter, bakterier og sopp, men ikke hos dyr. Den har fått navn etter det japanske navnet shikimino-ki for planten kinesisk stjerneanis (Illicium religiosum, Illiciaceae). Biosynteseveien fører fram til de 3 aromatiske aminosyrene fenylalanin, tyrosin og tryptofan.
Metabolismeveien starter med erythrose-4-fosfat som kommer fra pentosefosfatveien, og fosfoenolpyruvat fra glykolysen. Det første produktet er 3-deoksy-D-arabinoheptulosonsyre-7-fosfat (DAHP) katalysert av 3-deoksy-D-arabino-heptulosonat-7-fosfat syntase. Dette første enzymet blir ikke hemmet av noen av de aromatiske aminosyrene. Deretter følger en defosforylering, tilføring av vann og reduksjon med NADPH som gir shikimat. Shikimat fosforyleres med ATP og reagerer med fosfoenolpyruvat og danner 3-enolpyruvylshikimat-5-fosfat (EPSP).Enzymet 5-enolpyruvul-shikimat-3-fosfat syntase (EPSPS) katalyserer overføring av enolpyruvyl delen av fosfoenolpyruvat til shikimat-3-fosfat hvor man får dannet chorismat. Dette enzymet hemmes av ugrasmiddelet glyfosat.
Chorismat er greiningspunkt og siste felles forbindelse mellom tryptofan og fenylalanin/tyrosin. Chorismat omdannes til prefenat, katalysert av chorismat mutase, som videre ved transaminering gir arogenat. Arogenat gir tyrosin etter dekarboksylering katalysert av arogenat dehydrogenase. Arogenat kan også ved dekarboksylering og fjerning av vann gi fenylalanin, katalysert av arogenat dehydratase. Det finnes to isoenzymer av chorismat mutase. En type hemmes av tyrosin og fenylalanin, og aktiveres av tryptofan. Det andre blir ikke regulert ved tilbakekobling. Arogenat dehydratase hemmes av fenylalanin og aktiveres av tyrosin. Arogenat dehydrogenase hemmes av tyrosin. I biosynteseveien til tryptofan med en indolring omdannes chorismat til anthranilat katalysert av anthranilat syntase, med glutamin som aminodonor. Deretter følger 5 enzymatiske trinn hvor indolringen lages. Tryptofan benyttes også til å lage auxin, alkaloider og fytoaleksiner.
Alle trinnene i syntesen av aromatiske aminosyrer skjer i plastidene, men isoenzymer i synteseveien finnes også i cytosol. Biosynteseveien kan aktiveres ved stresstilstander.