Aminosyrer
Aminosyre (gr. Ammon - referer seg til den Egyptiske solguden hvor i nærheten av dennes tempel ble laget ammoniumsalter fra kamelmøkk). Aminosyrer er en gruppe organiske stoffer som har en aminogruppe og en karboksylsyregruppe festet til et alfa-karbonatom (karbonatom 2). Proteinaminosyrene er alfa-aminosyrer, untatt aminosyren prolin hvor alfa-karbonet er en del av en ringstruktur. Alfa-karbonatomet er chiralt (danner speilbilder), og kan derfor, unntatt glycin, finnes i to enantiomere, henholdsvis L- og D-form.
Tyve forskjellige aminosyrer brukes som byggestein eller byggestoff for protein.
Aminosyrene er amfolytter og skifter ladning avhengig av pH, og alle er av strukturen H2N-RCH-COOH, hvor R står for en sidegruppe som er forskjellig for de forskjellige aminosyrene. Ved aminosyrens isoelektriske punkt er det et likt forhold mellom anion- og kationformer av aminosyren, og aminosyren eksisterer som et nøytralt dipolart zwitterion (ty. switter - hybrid). Ved høyvolts papirelektroforese ved pH=5 vil sure aminosyrer f.eks. aspartat være negativt ladet og bevege seg mot den positive elektroden (anoden) og den basiske aminosyren lysin vil være positivt ladet og bevege seg mot den negativt ladete elektroden (katoden). Det finnes også en rekke ikke-protein aminosyrer i planter.
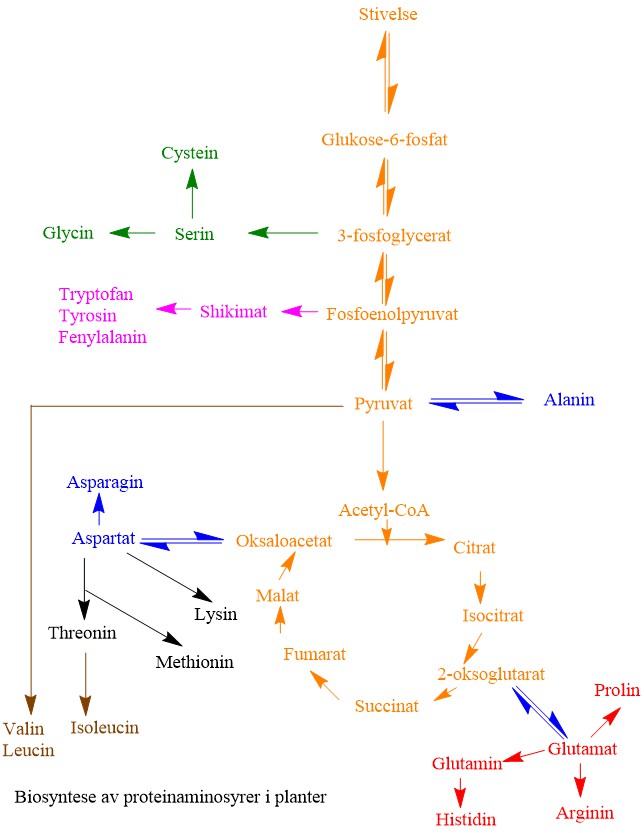
Biosyntese hos aminosyrer hos planter. I bakterier er det lignende biosynteseveier.
Hovedtyper proteinaminosyrer
Avhengig av sidekjeden kan aminosyrene organiseres i grupper: Følgende aminosyrer er hydrofobe (ikke- polare) (Tre-bokstav og en-bokstavforkortelsen angitt i parentes): alanin (ala; A), isoleucin (ile; I), leucin (leu; L), metionin (met; M), cystein (cys, ), fenylalanin (phe, F), prolin (pro; P), tryptofan (trp; W), og valin (val; V). De hydrofobe aminosyrene finnes ofte i det indre av proteinstrukturen.
Følgende aminosyrer er polare og uladet: asparagin (asn; N), cystein (cys; C), glutamin (gln; Q), glycin (gly; G), serin (ser; S), threonin (thr; T) og tyrosin (tyr; Y).
Polare og positivt ladet (+) ved fysiologisk pH (basiske aminosyrer) er: arginin (arg; R), histidin (his; H) og lysin (lys; L).
Polare og negativt ladet (-) ved fysiologisk pH (sure aminosyrer) er: asparaginsyre (asp; D) og glutaminsyre (glu; E).
Aminosyrene, untatt glycin, har alfa-karbonet som et stereosenter slik at det er mulig for aminosyrene å være i to enantiomere former.
De vanlig forekommende aminosyrene er L-aminosyrer (L-stereoisomer), men det finnes også noen D-aminosyrer, blant annet i peptidoglykan bakterieveggen, i noen antibiotika og i menneskehjernen i form av D-serin, D-alanin og D-aspartat.

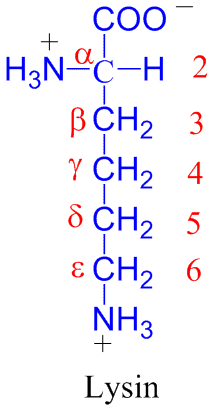
Kjemiske formel for proteinaminosyrer.
Aminosyrer består av en aminogruppe (-NH2) og en karboksylgruppe (-COOH) festet til det første karbonatomet, alfa-karbonet (2-), med i tillegg en polar eller upolar (hydrofob) sidekjede (-R) spesifikk for hver aminosyre (H2NCHRCOOH). Aminosyrer har amfiprotiske (ty. zwitterion, hermafroditt, hybrid) egenskaper hvor –NH2 kan være protonisert +NH3 , og –COOH deprotonisert –COO-.

De optiske egenskapene ved dreining av planpolarisert lys er egentlig tilknyttet glyceraldehyd med chirale egenskaper (speilbilder, enantiomere, R-rectus, S-sinister). Aminosyrer og peptider får grunnet zwitterionegenskapene et isoelektrisk punkt.
Aminosyrefamilier
Aminosyrer kan bli delt inn i familier avhengig av hvordan de blir laget i metabolismen: aspartatfamilien, aromatiske aminosyrer, glutamatfamilien, Det er ni essensielle aminosyrer som bare planter og bakterier kan lage, og disse må tilføres via kosten enten ved å spise plantemateriale eller kjøtt fra plantespisere.
Kromatografering
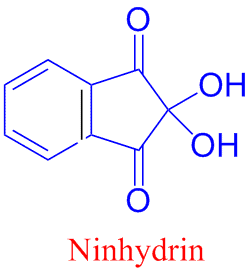
Det var den tyske kjemikeren Emil Hermann Fischer (1852-1919) som viste at proteiner bestod av sammenkoblede aminosyrer. Hydrolyse av peptider, deretter todimensjonal papirkromatografering (Whatman nr. 3 filtrerpapir) etterfulgt av farging med ninhydrin som gir blå eller purpurfargete flekker (unntatt prolin) i reaksjon med aminosyrer, var et viktig fremskritt for å kunne identifisere hvilke aminosyrer som inngikk i et peptid. I reaksjon mellom aminosyrer og ninhydrin frigis CO2. Ninhydrin kan også brukes til å påvise fingeravtrykk som skyldes aminosyrene man har på hendene., gir fiolett fargemønster av rillene. Aminosyrer gir vanligvis lillafargede produkter i reaksjon med fargestoffet ninhydrin. Aminosyrer kan også reagere med o-phtaldialdehyd og gi fluorescerende produkter som kan atskilles ved høytrykksvæskekromatografi.
Ekstraksjon av aminosyrer fra plantemateriale
Plantemateriale gnis ut i en morter i 0.1 N HCl i 70% etanol (0.5 g plantermateriale til 5 ml ekstraksjonsløsning. Til dette ekstraktet kan eventuelt norvalin eller norleucin tilsettes som standard. Ekstraktet sentrifugeres og supernatanten appliseres på en fastfase sterk kationbytter (SCX, 100 mg) som er kondisjonert med 2 ml 70% etanol i 0.1 N HCl. I avtrekk elueres aminosyrene ut med 1 mM 2M NH4OH. Damp forsiktig inn i avtrekk og løs i 0.5 ml 70 % etanol.
OPA-derivater av aminosyrer
I en HPLC med fluorescensdetektor og reversfase RP-18 kolonne kan man analyser og kvantifisere aminosyrer som OPA -derivater. Norvalin kan brukes som intern standard. OPA (o-phtalaldehyd bestående av benzenring med to aldehydgrupper) løst i etanol reagerer med primære aminer (R- NH2) i alkalisk løsning (boratbuffer pH 9.5) tilsatt 2-merkaptoetanol (HS-CH2CH2OH, helseskadelig) som til sammen danner et fluorescerende produkt. Aminosyren prolin kan ikke detekteres direkte med denne metoden, men må først blir oksidert med hypokloritt (NaOCl).
D-aminosyrer i bakterier
Amnosyrer med chiralt senter finnes både som D- og L- isomere.D-aminosyrene D-alanin og D-glutamat finnes i peptidoglykan i celleveggen hos bakterier. Noen typer antibiotika inneholder både D- og L-minosyrer slik som gramicidin, valinomycin bacitracin og tyrocidin.
Aminosyrene unntatt glycin har et eller to assymetriske karbonatomer og kan finnes i to enantiomere former og optiske isomere som L-aminosyre og D-aminosyre, hvor α-karbonatomet er chiralet eller asymmetrisk bestemt av hvor aminogruppen er plassert. I Fischerprojeksjon er aminogruppen plassert il venstre i L-formen og til høyre i D-formen. I proteiner hos eukaryoter og prokaryoter er det vanligvis L-formen av aminosyrer som inngår, men hos bakterier finnes isomeren D-aminosyrer som i celleveggen og peptidoglykan hvor man kan finne både D-glutamat og D-alanin. D-aminosyrer blir laget fra L-aminosyrer katalysert av enzymet aminosyre racemase som bruker vitamin B6 pyridoksalfosfat, et B-vitamin som kofaktor. Bacitracin, et et peptidantibiotikum inneholder D-aminosyrer. Det samme gjelder D-sykloserin og aktinomycin D isolert av fra slekten Streptomyces. Noen marine snegl bruker D-aminosyrer som toksin. Man kan spekulere om hvorfor L-aminosyrer ble valgt under evolusjonen for å inngå i proteiner.
D-aminosyrer i pattedyr
L-aminosyrer er det som inngår i proteiner i vanlig proteinsyntese, men man har funnet at i menneske hjernen finnes det både D-serin, D-alanin og D-aspartat, men i lavere konsentrasjon enn de tilsvarende L-formene. D-serin er en ko-agonist til den eksitatoriske glutamatreseptoren N-metyl-D-aspartat (NMDA) og har en modulerende regulering av denne reseptoren.
Enzymer som deltar i dannelsen og omsetning av D-aminosyrer er aminosyre racemace og D-aminosyre oksidase. D-aminosyrer blir laget via en racemisering av L-enantiomeren katalysert av pyridoksalfosfatenzymet aminosyre racemace.
L-aminosyre ⥢ D-aminosyre
D-aminosyre oksidase hos mennesker er et flavoprotein som inneholder FAD og deltar i oksidativ deaminering av D-aminosyrer. D-minosyre oksidase katalyserer en reaksjon som danner en α-ketosyre 2-oksokarboksylat, ammoniakk (NH3) og hydrogenperoksid (H2O2):
D-aminosyre + + O2 + H2O → 2-oksokarboksylat + NH3 + H2O2
Enzymet er også funnet i nyrer
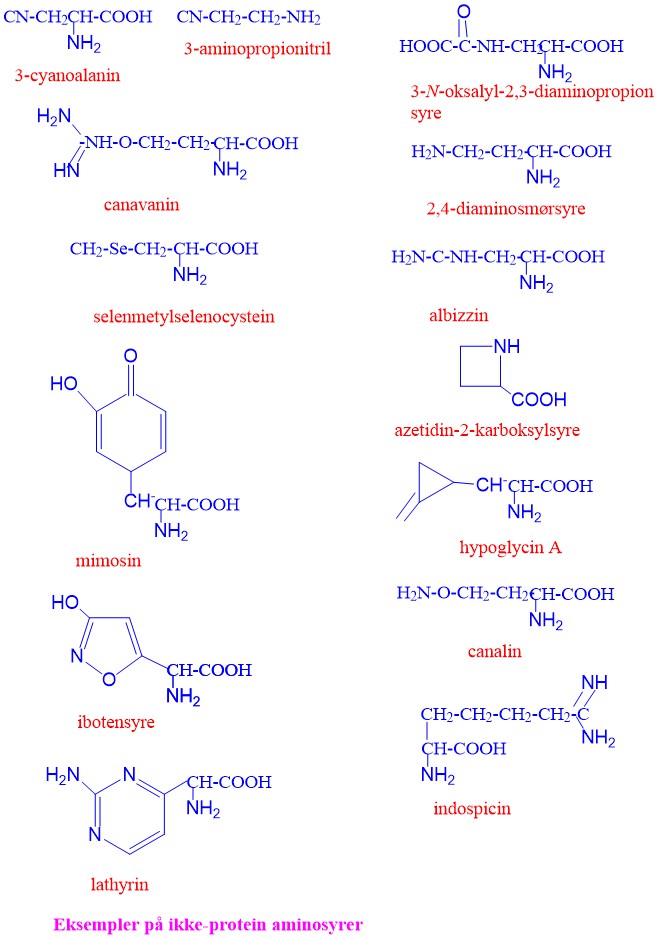
Noen ikke-proteinaminosyrer
Litteratur
Wikipedia