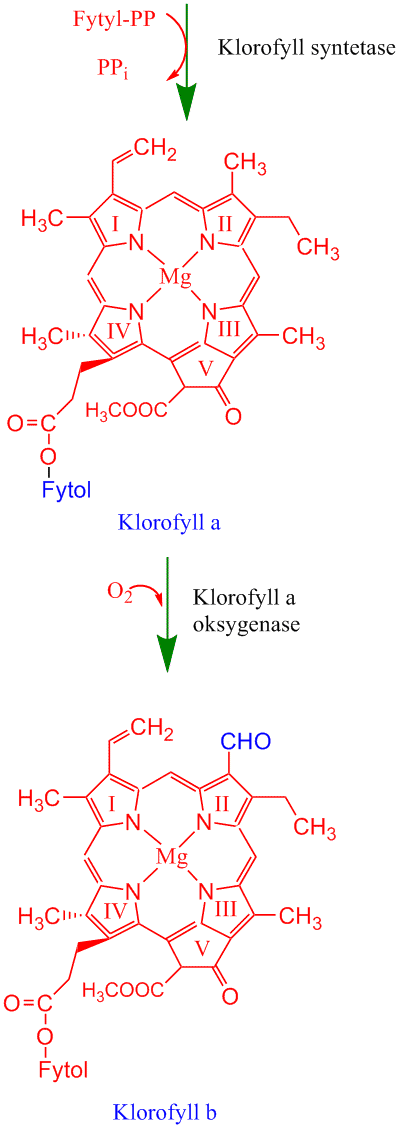
Består av en tetrapyrrolring (porfyrin) med konjugerte karbon dobbeltbindinger med magnesium chelatert i midten av ringen, samt en hale av fytol (20-karbon alkohol) festet til ringen (ring IV) med en esterbinding. Klorofyll mottar lysenergi i fotosyntesen i en klorofylleksitasjon. Det er fire kjente utgaver av klorofyll: a, b, c og d, dessuten bakterieklorofyll fra anaerobe fotosyntetiserende bakterier. Klorofyll a er det primære fotosyntesepigmentet i planter, alger og blågrønnbakterier.
Klorofyll b lages fra klorofyll a og har en aldehydgruppe, formylgruppe (-CHO) på ring II istedet for en metylgruppe (-CH3) som i klorofyll a, og er et hjelpepigment (aksesorisk pigment, antennepigment). I proklorofytter som Prochlorococcus inneholder divinyl-klorofyll b (klorofyll b2) og divinyl-klorofyll a (klorofyll a2)
Klorofyll c mangler fytolhalen og finnes i diatoméer, dinoflagellater og brunalger.
Klorofyll d er bare funnet i rødalger og en O-CHO gruppe erstatter -CH=CH gruppe på ring I. Klorofyll d er også funnet i en Prochloron-lignende prokaryot Acaryochloris marina.
Bakterieklorofyll er klorofyll fra fotosyntetiske bakterier som purpurbakterier og grønne bakterier, unntatt blågrønnbakterier som i stedet inneholder fykobiliproteiner (fykoerytrin, fykocyanin og allofykocyanin) . Bakterieklorofyll a atskiller seg fra klorofyll a i planter ved å ha en av pyrrolringene i mer redusert form og en vinylgruppe erstattes av en acetylgruppe. Bakterieklorofyll absorberer i blått ved bølgelengde 367 nanometer (nm), og ved lengre bølgelengder i rødt og infrarødt enn klorofyll, splittet i tre ca. 800 nm, 850 nm og 890 nm, slik at de to absorbsjonsbåndene er lenger fra hverandre enn i klorofyll. Det er også funnet bakterieklorofyll som absorberer kortbølget infrarødt ved ca.1014 nm. Det er både bakterieklorofyll a og bakterieklorofyll b. Grønne svovelbakterier som Chlorobium inneholder Chlorobium-klorofyll (bakterioviridin), mens purpurbakteriene inneholder mest bakterieklorofyll
Klorofyllid er et klorofyllmolekyl hvor fytol-halen er fjernet ved hydrolyse. Feofytin er et klorofyllmolekyl hvor magnesium (Mg2+) i kjernen er fjernet. Feofytin er den formen av klorofyll som mottar elektroner fra eksitert reaksjonssenterklorofyll P680 og fanger og fikserer derved lysenergien. Fjernes i tillegg fytolhalen fra feofytin dannes feoforbid.
De dekkfrøete blomsterplantene (angiospermene) lager ikke klorofyll i mørke, og gir etiolerte planter Det skyldes at protoklorofyll a, forkomponenten til klorofyll må reduseres, og dette skjer vha. enzymet NADH:protoklorofyll oksidoreduktase som er et enzym som trenger lys. Protoklorofyllid mangler dobbelbinding mellom to karbonatomer i en av de fire pyrrol-ringene. Den kan absorbere lys, men er ikke grønnfarget. Hos de nakenfrøete (gymnospermene) skjer reduksjonen uavhengig av lys, og plantene blir grønne også i mørke. Det samme skjer også i karsporeplanter og moser. Den lange hydrokarbon fytolhalen gjør at klorofyll er lite løselig i vann, men er lett løselig i lipidmembranen i tylakoidene. Klorofyll løst i et organisk løsningsmiddel har andre absorbsjonsmaksima enn klorofyll- proteinkomplekser i tylakoidmembranene i kloroplasten i en intakt plante. Klorofyll har to sterke absorbsjonsbånd, absorberer lys sterkt i rødt og blåfiolett og mindre i grønt (490-550 nm), derav den grønne fargen. Liten absorbsjon av lys i midten av den synlige delen av spektret, i det grønne, blir kompensert ved at bladene forekommer ofte i flere sjikt og da blir også det grønne lyset absorbert. Det grønne lyset er også det som trenger lengst inn i et blad. Den første absorbsjonstoppen i blått kalles Soret bånd (Jacque-Louis Soret) som skyldes \(\pi -\pi^*\) transisjon. F.eks. klorofyll a har et absorbsjonsmaksimum i rødt lys i løsning ved 663 nm, men ved ca. 680 nm i et intakt blad. I klorofyll b er de to absorbsjonsbåndene tettere sammen( klorofyll har maksimal absorbsjon ved ca. 460 nm og 650 nm i organisk løsningsmiddel, mens tilsvarende for klorofyll a er ca. 430 nm og 660 nm), og gjør det mulig å overføre eksitasjonsenergi i den røde delen av spektret fra klorofyll b til klorofyll a. Det er indikasjoner på at hos noen organismer kan det finnes klorofyll med chelatert zink istedet for magnesium. Biosyntese av klorofyll (C55H70MgN4O6). Man vet ikke helt funksjonen til chelatert magnesium (Mg2+) i klorofyll, og det kan ikke skifte valens slik som jern i hem i en toverdig og treverdig form.
Eksitert reaksjonssenterklorofyll er en kraftig elektrondonor
Eksitert reaksjonssenterklorofyll er en spesiell type klorofyll a i reaksjonssenteret omgitt av lyshøstende aksessoriske pigmenter, P680 i fotosystem II (feofytin-kinon reaksjonssenter) og P700 i fotosystem I (jern-svovel reaksjossenter). I fotosystem II vil eksitert reaksjonssenterklorofyll P680* , en sterk oksidant og elektrondonor, avgi et elektron til feofytin, hvor det skjer en fotooksidasjon og ladningsseparasjon: P680* + feofytin → P680+ + feofytin-. P680+ er sterkt oksidert og mottar elektroner fra oksidasjon av vann og gjendannes, klar for ny eksitasjon og ladningsseparasjon: P680+ + elektron → P680. Elektronet som feofytin har mottatt overføres videre til kinon QA: feofytin- + QA → QA- . Elektronet fraktes videre via QB bundet til D1-proteinet. Plastokinon (PQ) kan motta to elektroner (PQ2-) og to protoner og danner PQH2 (plastokinol) som diffunderer gjennom membranen til cytokromb6f, og elektronet overføres vi kobberproteinet plastocyanin før det kommer fram til reaksjonssenteret i fotosystem I. Eksitert reaksjonssenterklorofyll i fotosystem I, P700* overfører elektronet til fyllokinon (et K1-vitamin) og videre vide jern-svovel (Fe4S4) til ferredoksin videre til NADP+ og danner reduksjonskraften NADPH2.
For mye lys kan skade fotosystemene
Mye lys kan gi skader i fotosynteseapparatet med tilhørende fotoinhibering og skader i D1-proteinet. VAZ-syklus og luten kan fjerne eksitasjonsenergi i form av varme. Plantene kan beskytte seg mot mye lys via konformasjonsendringer og transisjoner i de lyshøstende klorofyllkompleksene (LHCII). Redoksnivået til plastokinon virker som et signal på reduksjonsnivået. Ved sterk redusering av plastokinon og dannelse av mye PQH2 så aktiveres en LHCII kinase og fosforyleringen blokkerer for overføring av eksitasjonsenergi til fotosystem I. Spesielt mye skader oppstår i planter som er adaptert til lite lys og som utsettes for mye lys, f.eks. bunnvegetasjon i en skog etter hogst, eller planter i en mørk stue som plutselig utsettes for mye direkte lys. Fotosystemene kan også skades hvis det er mye lys ved lav temperatur.
Vann - vannsyklus i fotosyntesen
Elektroner fra oksisk fotosyntese kommer fra vann. Oksygen er imidlertid et sterkt elektronegativt grunnstoff som trekker på elektroner. Elektroner fra vann som har kommet fram til fotosystem I kan bli overført til oksygen og det blir dannet superoksid anionradikalet av oksygen (O2•-). Superoksid dismutaser er effektive enzymer som fjerner oksygenradikaler og danner hydrogenperoksid (H2O2). Hydrogenperoksid er også en potensiell skadelig form og omsettes videre via enzymet askorbat peroksidase og det dannes vann. Mehler-reaksjonen. Imidlertid har hydrogenperoksid og oksygenradikaler viktig funksjon i beskyttelse mot bakterier og andre patogener, og kan også inngå i signalveier i plantene.
Flavoidjernproteiner deltar i fotobeskyttelse hos blågrønnbakterier
Flavodijernproteiner kan fotoredusere oksygen (O2) til vann (H2O) uten at det dannes skadelige reaktive oksygenforbindelser. Disse proteinene er spesielt viktig når lysmengden til fotosyntesen er sterkt varierende. Under evolusjonen ble dette beskyttelsessystemet erstattet av andre former.
Grunnen til at klorofyll har grønn farge og kan bli eksitert av bølgelengder tilsvarende synlig lys
Organiske ringstrukturer med konjugerte dobbeltbindinger, det vil si alternerende karbon dobbeltbindinger og karbon enkeltbindinger, er stabilisert via resonans. Vi kan starte med benzen, C6H6 som har to resonansstrukturer for tre dobbeltbindinger og tre enkeltbindinger:
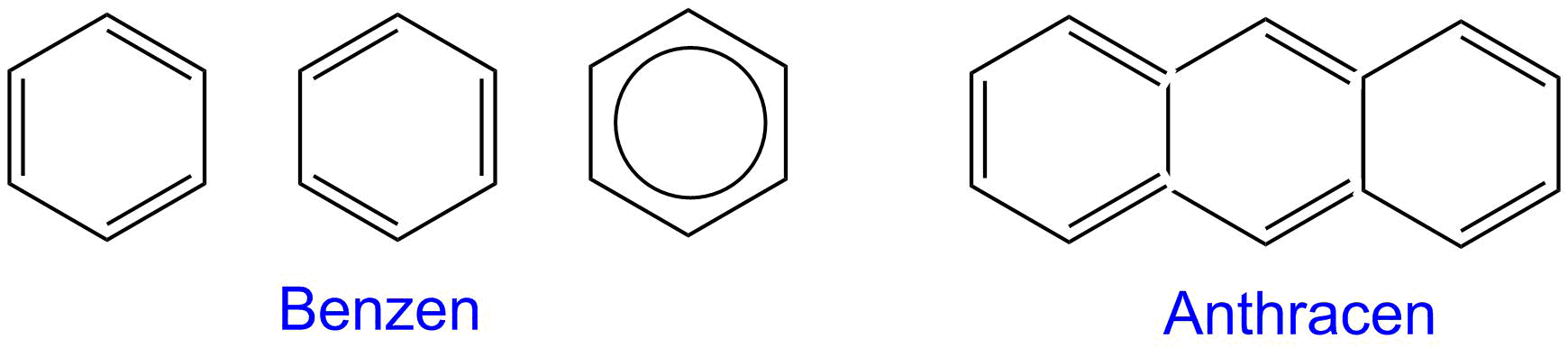
Anthracen, et stoff som kan utvinnes fra steinkulltjære, blir brukt som basis for syntetiske fargestoffer som alizarin, og er vist med en av resonansstrukturene. Jo flere dobbeltbindinger desto mer skifter absorbsjonen av elektromagnetisk stråling mot synlig lys. Benzen har et absorbsjonsbånd som er mindre enn 250 nm, mens for anthracen absorberer lengre bølgelengder, men er fremdeles uten farge. Konjugerte dobbeltbindinger gjør at de eksiterte energinivåene til elektronene splittes i flere nivåer og det blir mindre energisprang mellom grunnivå og eksitert nivå
Ser man på porfyrinkjernen med de fire tetrapyrol-ringene i klorofyll, så observerer man i alt 12 konjugerte karbon-karbon dobbeltbindinger alternerende med karbon-karbon-enkeltbindinger - C-C=C-C=C-C=C-C=C-. Disse er resonansstabilisert av - C=C-C=C-C=C-C=C-C=. I karbon-dobbeltbindingene er det delokaliserte pi-elektroner (\(\pi\)-elektroner) i molekylorbotaler, i alt 24 pi-elektroner. I hvert pi-orbital er det to elektroner med motsatte spinn. Det betyr at for eksitert klorofyll er det to eksiterte nivåer, 2. singlett hvor blått lys har nok energi til å eksitere, og 1. singlett, et lavere nivå hvor rødt lys har nok energi. Det kalles singlett-nivåer siden det eksiterte elektronet og elektronet som blir igjen i grunntilstanden har motsatt spin. Levetiden for 2. singlett er meget kort, og elektronet faller ned til første singlett og kvitter seg med energiforskjellene mellom disse to nivåene i form av varme. Dette er grunnen til at fluorescensen fra en klorofyll-løsning f.eks. klorofyll løst i aceton får rød fluorescens, enten man belyser med blått eller rødt lys. Klorofyll i grunntilstand og eksitert nivå har flere vibrasjonsnivåer og noe av eksitasjonsenergien blir tapt (Stokes skift, som angir forskjell i absorbsjonsspekter og emisjonsspekter tilsvarende ca. 20-25 nanometer).
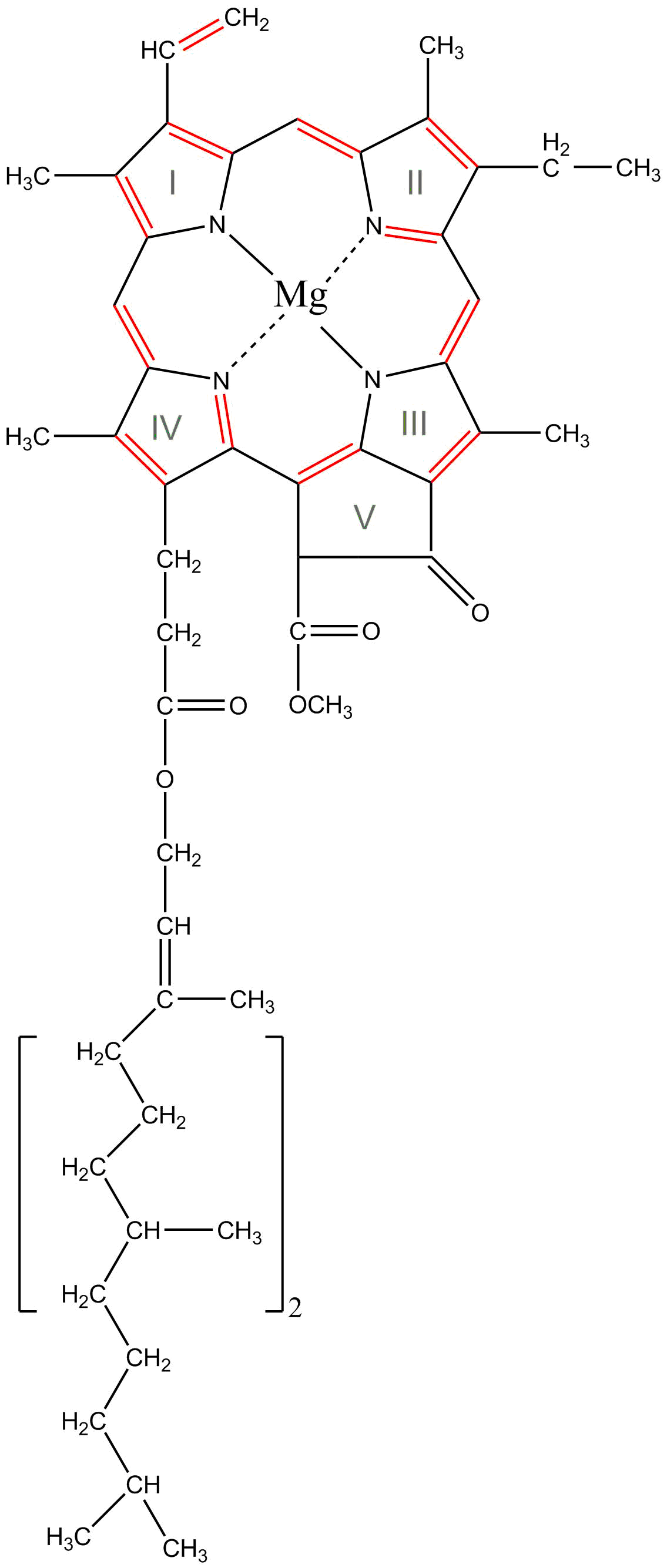
Kjemisk strukturformel klorofyll a. De tyske kjemikerne Richard Willstätter og Hans Fisher fikk nobelprisen i kjemi for oppklaring av strukturen, og Robert B Woodward fikk nobelprisen for syntese av klorofyll. Klorofyll b har -CHO i ring II i stedet for -CH3. En vinylgruppe (-CH=CH2) er festet til ring I. En C15 fytolhale i ring IV, bygget opp av isopren, 14 enkeltbindinger og en dobbeltbinding, binder klorofyll til tylakoidmembranen. Klorofyll er også festet til klorofyllbindende proteiner.
Delokaliserte elektroner gir resonansstabilisering av molekylet, og jo flere -C=C- desto mindre energi trenger lyset for å kunne eksitere molekylet. Et pi-elektron i grunntilstanden som blir truffet av et foton blir eksitert til et pi-antibindende orbital (\(\pi^*\)). Denne eksitasjonsenergien kan bli overført til andre klorofyllmolekyler ved resonans, hvor eksitasjonsenergien til slutt havner i et reaksjonssenterklorofyll, P680 i fotosystem II som kan avgi et elektron til elektronakseptor, feofyting. Det avgitte elektronet blir erstattet med et elektron som kommer fra oksidasjon av vann. Blå og røde fotoner blir mest effektivt absorbert, og derfor ser klorofyll grønnfarget ut for vårt øye og hjerne. Eksiteringen er en HOMO-LUMO transisjon.
Ser man på den kjemiske formelen for karotenoidet beta-karoten er det i alt 11 konjugerte karbon-karbon dobbeltbindinger og molekylet blir guloransje når blått lys blir absorbert. Hem i hemoglobin har jern chelatert i porfyrinringen i stedet for magnesium som i klorofyll. Hem har 13 karbon-karbon dobbeltbindinger med i alt 26 pi-elektroner og er et rødfarget molekyl. I alle organiske pigmenter som har farger, inkludert fytokrom, anthocyaniner og melaniner, så finner man disse alternerende -C=C-C=C- som gjør at synlig lys har nok energi til å eksitere molekylet, noe av lyset blir absorbert og resten blir reflektert eller transmittert.
Triplett klorofyll
Eksitert singlett klorofyll ( 1klorofyll*) kan i noen tilfeller ved spinreversering danne eksitert triplett klorofyll (3klorofyll*), hvor det eksiterte elektronet har samme spinretning som det gjenværende elektronet i elektronparet i grunntilstand i klorofyll. Triplett klorofyll har lang nok levetid til å kunne overføre eksitasjonsenergien sin til oksygen og danne reaktivt singlett oksygen (1O2). 1klorofyll* → 3klorofyll*. Deretter: 3klorofyll* + 3O2 → 1klorofyll + 1O2. Singlett oksygen gir oksidative skader i cellene En av oppgavene til karotenoidene er å fjerne energien til elektronet i 2\(\pi\)-antibindende orbital (\(\pi^*\)) i singlett oksygen i form av varme, og mer stabilt triplett oksygen (3O2) blir dannet. Dette prinsippet med pigment, lys og triplett oksygen og overføring av eksitasjonsenergi og dannelse av singlett oksygen kalles fotodynamiske effekter, og blir også anvendt innen medisin.
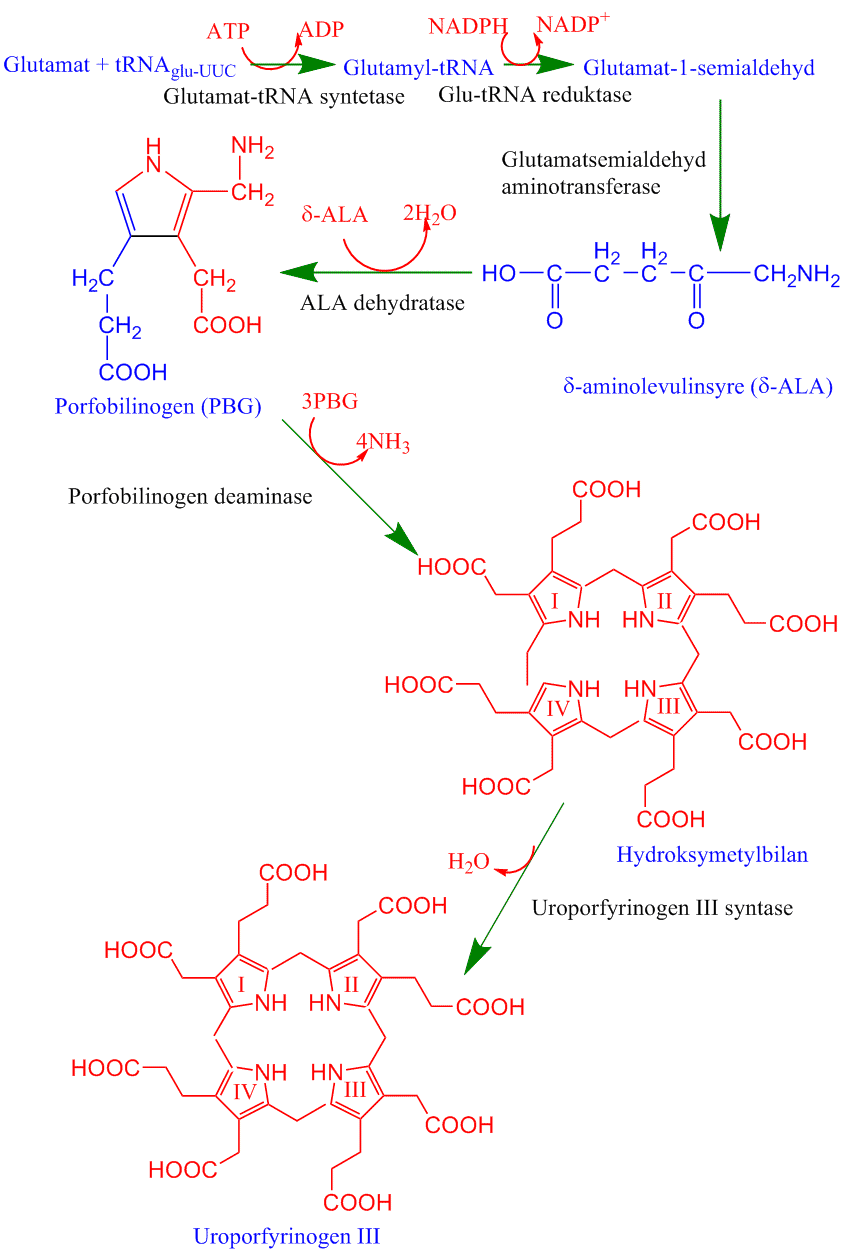
Biosyntese av klorofyll og hem
Klorofyll og hem er bygget opp av tetrapyrrol med start fra aminosyren glutamat (glutaminsyre) via \(\delta-\)aminolevulinsyre. Porfyrin-kjernen er i størrelsesorden 1.5x1.5 nanometer og fytolhalen har lengde ca. 2 nanometer (nm).
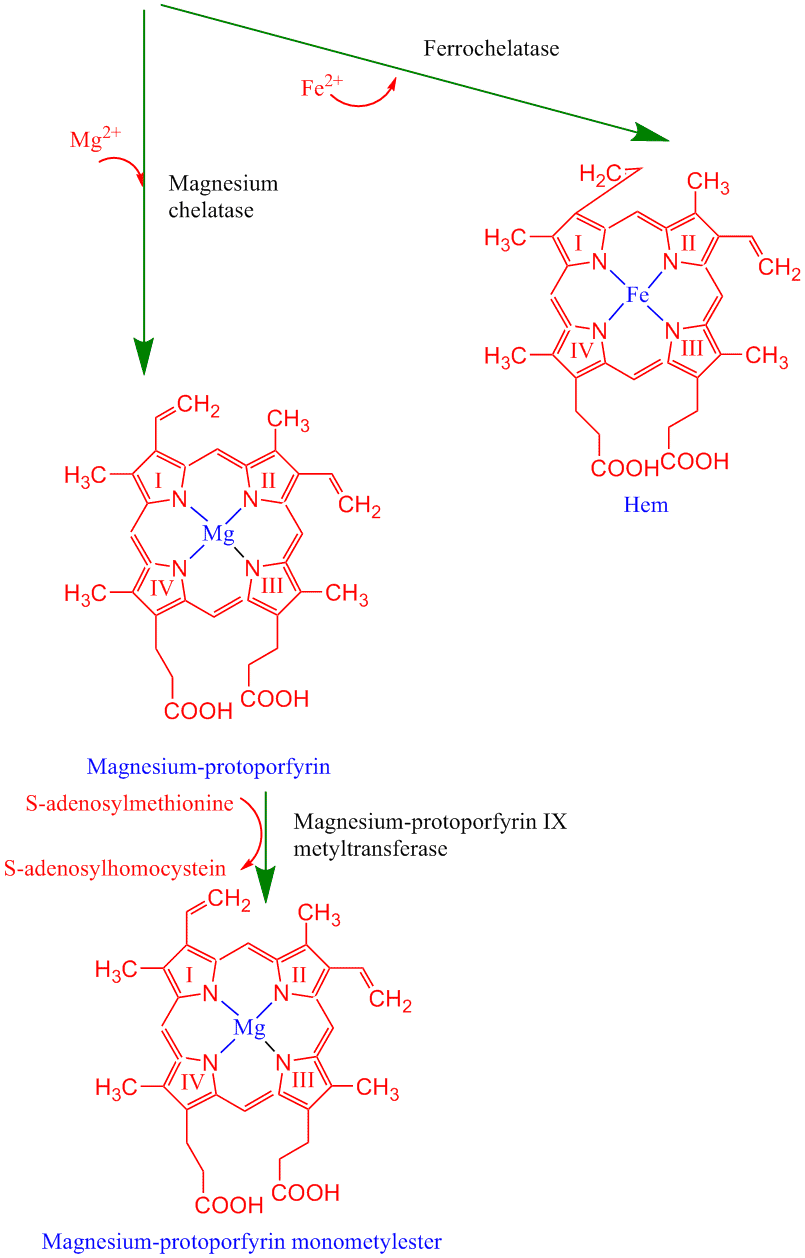
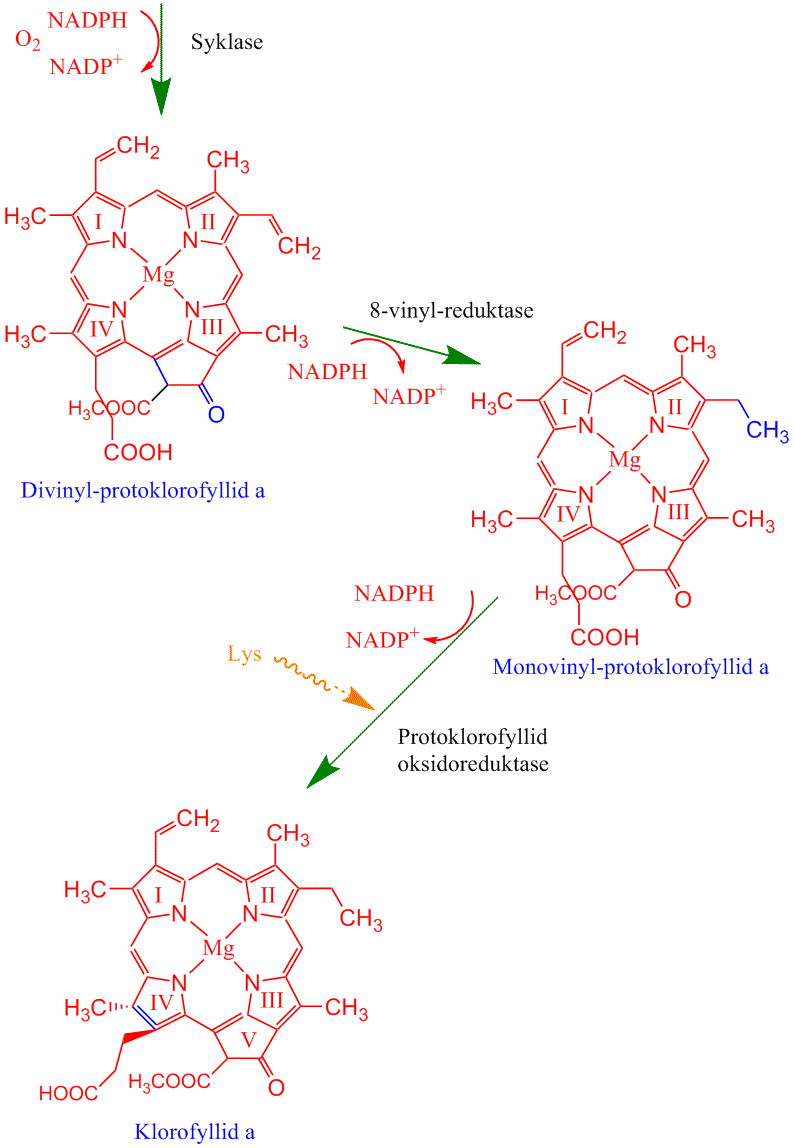
Mengden klorofyll i plantene er regulert. Klorofyll er et tetrapyroll (porfyrin) og deler flere biosyntesetrinn med hem, som brukes til cytokromer. Det sendes et signal fra plastide til kjerne om start av klorofyllsyntese. Klorofyll lages fra aminosyren glutamat. δ(5)-aminolevulinsyre (ALA) lages fra glutamat via 2-oksoglutarat og 2,5-dioksovalerat i en prosess koblet til tRNAglu katalysert av glutamyl-tRNA reduktase. Porfobilinogen som gir utgangspunkt for pyrrolringene i klorofyll lages fra to molekyler ALA katalysert av ALA dehydratase. Fire pyrrolringer gir protoporfyrin IX og til hit danner felles biosyntesevei for hem og klorofyll. Deretter settes Mg2+ inn i kjernen av molekylet katalysert av en Mg-chelatase på biosynteseveien til klorofyll. Fe2+ settes inn hvis det skal lages hem katalysert av ferrochelatase. De videre trinnene i klorofyllsyntesen er at Magnesium protoporfyrin IX metyleres og blir deretter omdannet til protoklorofyllid ved at det dannes en 5. ring av en propionsyresidekjede. Protoklorofyllid fotoreduseres til klorofyllid katalysert av det lysavhengige enzymet protoklorofyllid oksidoreduktase, og finnes hos blågrønnbakterier, grønnalger, moser, gymnospermer og angiospermer. Det finnes også en lysuavhengig reduksjon av protoklorofyllid, som anses for å være en mer primitiv, og finnes hos purpurbakterier, grønnalger, moser og gymnospermer. Siste trinn i klorofyllsyntesen er påhekting av en hydrofob C20 fytolhale, katalysert av enzymet klorofyll syntetase. Fytolhalen lages via geranylgeranyl reduktase som katalyserer reduksjonen (hydrogenering) av geranylgeranyldifosfat til fytyldifosfat. Fytyldifosfat kan brukes både til å lage fytolhalen på klorofyll og til syntese av α-tokoferol. Klorofyll a kan omdannes til klorofyll b katalysert av en klorofyll oksygenase som omdanner en metylgruppe til en formylgruppe. Denne endringen gir relativt store forandringer i absorbsjonsegenskapene. Klorofyll er grønnfarget fordi blått og lys absorberes mer effektivt enn grønt.
Chelatering med jern i protoporfyrin IX ga som tidligere nevnt hem. Hem oksygenase omdanner hem til biliverdin IXα katalysert av hem oksidase. Biliverdin IXα omdannes til 3Z-fytokromobilin katalysert av fytokromobilin syntase. En isomerisering gir deretter 3E-fytokromobilin