CO2 blir assimilert (tatt opp) organsimer som kan utføre fotosyntese
CO2 blir assimilert (CO2-fangst) i fotosyntesen hos autotrofe organismer (planteplankton, alger og planter), og blir utskilt ved cellerespirasjon i alle levende organismer på Jorden. Under anaerobe forhold blir CO2 produsert ved fermentering. Fotosyntesen assimilerer så store mengder CO2 at det gir sykliske svingninger av CO2-konsentrasjonen i atmosfæren, lav CO2-konsentrasjon ved aktiv fotosyntese i vekstsesongen, og høy konsentrasjon i vinterhalvåret.
I gassutvekslingen hos alle dyr, planter og mikroorganismer skilles det ut CO2 fra metabolisme av organisk materiale. I utåndingsluften fra mennesker er det ca. 5% CO2, og luften vi puster inn er det ca. 0.041% CO2. Det vil si at et menneske i gjennomsnitt og grovt regnet puser ut 0.36 tonn CO2 per år. Planter kan produsere CO2 ved vanlig cellerespirasjon og i fotorespirasjon. I tillegg til respirasjon blir CO2 dannet ved forbrenning av organisk materiale og fossilt brensel, fra vulkanutbrudd, varme kilder og geysirer.
I levende organismer kan enzymet karbonsyre anhydrase katalysere overgang mellom CO2 og HCO3-.
Rubisko og CO2-gjødsling
Rubisko er det enzymet som fikserer CO2, i natruens egen CO2-fangst, og rubiskproteinet finnes i enorme mengder, men siden dette enzymet har relativt lav affinitet for CO2 har evolusjonen utviklet en rekke metoder (C4-fotosyntese, karboksysomer) for oppkonsentrering av CO2 omkring rubisko, blant annet for å redusere fotorespirasjon. Selv dagens konsentrasjon av CO2 i atmosfæren gir ikke optimal fotosyntese, forutsatt at det andre vekstfaktorene er tilstede, blant annet nitrogen (gjødsel) og vann, slik at økning i CO2-konsentrasjon gir en CO2-gjødsling av den gjenlevende vegetasjonen. Kombinasjonen høy temperatur, økt CO2-konsentrasjon og nitrogen i form av oksidasjon av nitrogenoksider (NOx) til nitrat (salpetersyre) har gitt økt plantevekst hos C3-planter hvis det er nok vann tilstede. Eksperimentene som er gjort med CO2-gjødsling er gjort i drivhus i veksthusnæringen, og konsekvensene for den naturlige vegetasjonen er i mange tilfeller ukjent. Man vet f.eks. at økt CO2-konsentrasjon i atmosfæren gjør at det dannes færre spalteåpninger per arealenhet på bladene. C4-planter responderer annerledes på økt CO2 enn C3-planter. Fytoplankton, alger og vannplanter kan få endret fotosynteserespons grunnet pH-endringer i vannet og endrete karbonlikevekter. Det kan også være tilbakekoblingsmekanismer fra økt CO2 som vi ikke har helt skjønt rekkevidden av.
Kilder til CO2
Hovedkilden til CO2 i atmosfæren er cellerespirasjon, hos alle levende organismer (dyr, planter, sopp, og bakterier), vegetasjonsbrann og brenning av biomasse, brenning av fossilt brensel (kull i kullkraftverk, olje og gass i gasskraftverk og husoldning), sementproduksjon og vulkanutbrudd.
CO2-kompensasjonspunktet for C3-planter er ca. 0.01% CO2 (100 ppm), et resultat av fotorespirasjon, og man anslår laveste CO2 konsentrasjon som er nødvendig for å opprettholde livet på Jorden slik det er idag er ca. 0.02% (200 ppm).
Karbondioksid løst i vann virker som en svak syre, karbonsyre (H2CO3):
CO2 + H2O ⇔ H2CO3 ⇔ H+ + HCO3-
Brenning av alt materiale som inneholder karbon gir karbondioksid, eller karbon monoksid (CO) hvis det er dårlig tilgang på oksygen.
Store mengder karbondioksid er bundet i form av kalsiumkarbonat (CaCO3).
CO2 fra aerob cellerespirasjon
Når trekarbonforbindelsen pyruvat blir oksidert til CO2 skjer det i tre enzymatiske oksidative dekarboksyleringer. Samtidig blir NAD+ blir redusert til NADH. Elektronene i NADH blir i elektrontransportkjeden i mitokondriene videre omsatt til ATP. Cellerespirasjonen er koblet sammen med gassutveksling. Hos dyr i vann via akvatisk respirasjon.
I overgang fra glykolyse i cytoplasma til trikarboksylsyresyklus i mitokondriene blir pyruvat oksidert i en oksidativ dekarboksylering til acetyl-oenzym A, katalysert av enzymet pyruvat dehydrogenase:
pyruvat + CoASH + NAD+ → Acetyl-CoA + CO2 + NADH + H+
NAD+ blir redusert til NADH.
I mitokondriene skjer den andre oksidative dekarboksyleringen katalysert av enzymet isositrat dehydrogenase hvor isositrat blir oksidert til 2-oksoglutarat (α-ketoglutarat) og NAD+ blir redusert til NADH:
isositrat + NAD+ ⇌ 2-oksoglutarat + CO2 + NADH + H+
Den tredje oksidative dekarboksylering er katalysert av enzymet 2-oksoglutarat dehydrogenase som oksiderer 2-oksoglutarat til succinyl-koenzym A.
2-oksoglutarat + CoASH + NAD+ → succinyl-CoA + CO2 + NADH + H+
I oksidasjon av karbohydrater blir det laget pyruvat, mens i β-oksidasjonen peroksisomer blir fettsyrer fra fett oksidert till acetyl-CoA som ved videre oksidativ dekarboksylering gir to molekyler CO2. I tillegg til å bli brukt i oppbygging av proteiner kan aminosyrer brukes som energikilde omdannet til til acetyl-CoA og videre oksidert som vist over. Forholdet mellom mengden oksygen forbrukt og CO2 utskilt ved respirasjon kan bli uttrykt i form av en respirasjonskvotient.
Karbondioksid fra forbrenning (oksidasjon)
Oksidasjon kan skje ved biologisk temperatur katalysert av enzymer i organismene (metabolsk ksidasjon) , eller ved høy temperatur i forbrenningsreaksjoner. alt materiale som inneholder karbon, oksygen og hydrogen kan brennes og omsettes til energi, i tillegg produseres CO2 og vann. Det vil si alle typer søppel produsert fra menneskelig aktivitet, alle typer biomasse, inkluert skogbranner.
For eksempel brenning av metan (CH4), eller hvis metanotrofe bakterier omsetter metan
CH4 + 2O2 → CO2 + 2H2O + energi
Brenning eller cellerespirasjon av organiske stoffer som inneholder karbohydrater:
C6H12O6 + 6O2 → 6CO2 + 6H2O + energi
Brenning eller cellerespirasjon av stearinsyre:
C18H36O2 + 26O2 → 18CO2 + 18H2O + energi
Fett inneholder mye karbon og hydrogen og lite oksygen, og frigir derfor mye energi ved oksidasjon. I forbrenningsreaksjonen er energien i form av varme. Ved cellerespirasjonen blir energien produsert i form av reduksjonskraft (NAD(P)H), den biologiske energibæreren ATP, samt varme.
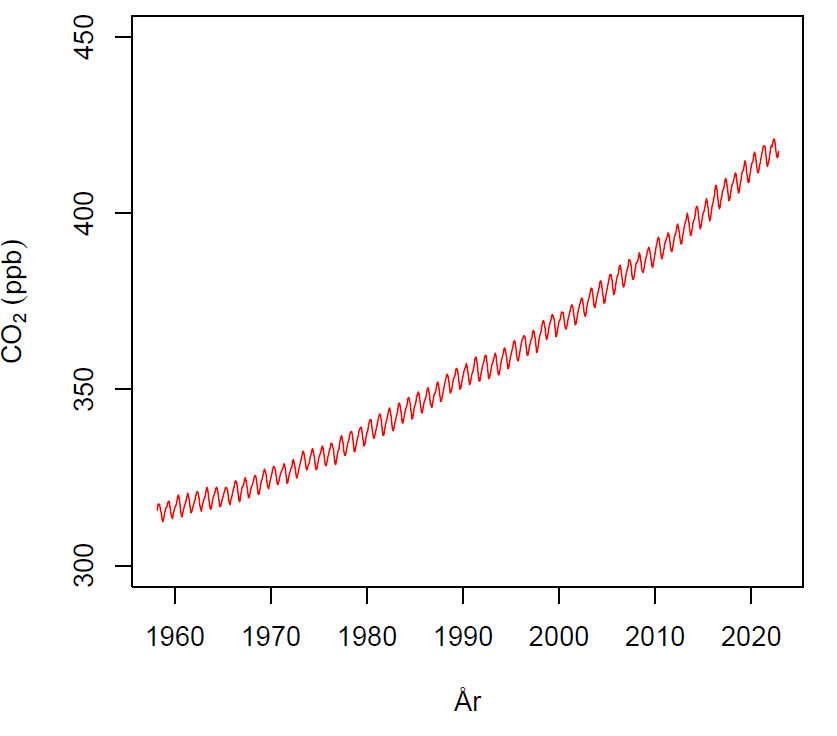
Keelingkurven som viser den kontinuerlige stiningen i CO2-konsetrasjonen i atmosfæren. Svingningene på kurven skyldes den sesongmessige variarisjon fotosyntesen på den nordlige halvkule.
Bunntråling frigir store mengder CO2
Fiske med bunntråling på havbunnen kan frigi store mengder CO2, anslått til 370 millioner tonn CO2 per år ifølge en forskningsartikkel i Fronteriers in Marine Science. Dette er en kilde til O2 som man har helt uteglemt. I tillegg gir bunntråling store skader på økosystemene tilknyttet havbunnen I perioden 1996-2000 er mengden ansaltt til .34-0.37 Pg CO2 år-1.
Bunntråling og utvinning av mineraler fra dyphavsbunn vil virvle opp partikkelskyer med uorganisk og organiske materiale som kan spre seg over store områder og få Når det organiske materialet i sedimentene kan komme i kontakt med oksygenrikt vann fra omrøringen og kunne gi meget store utslipp av CO2 med uanede konsekvenser for liv i dyphavet. Fytoplankton, alger og annet organiske materiale som synker ned på havbunnen har gjennom geologiske tidsperioder blitt omdannet til olje og gass, og viser at det kan dreie seg om store mengder.
Atwooed RB et al: Atmospheric CO2 emissions and ocean acidification from bottom-trawling. Front. Mar. Sci.2024 Volume 10 – 2023, doi.org/10.3389/fmars.2023.1125137
Karbondioksid fra produksjon av sement
Termisk nedbrytning av kalkstein (CaCO3), tidliger gjort i kalkovner, gir kalsiumoksid (CaO).Brent kalk (kalsiumoksid) framstilles ved oppvarming av kalkstein (CaCO3, kalkspat, kalsitt) i en kalkovn ved ca. 1000oC med følgende reaksjon:
CaCO3 → CaO + CO2
I sementovnene blir det produsert store mengder CO2, og sementovnene er også et sted man kvitter seg med alle typer organiske løsemidler, olje, maling og alt annet brennbart organisk avfall i væskeform.
Kalkmørtel er brent kalk (CaO) laget ved brenning av kalkstein (CaCO3), marmor eller skjell i en kalkovn tilsatt vann slik at det blir dannet lesket kalk (Ca(OH)2) i en kalkdeig som tilsettes ca. 5% sand. Den herdes ved opptak av CO2 fra lufta. Hvor kalsiumhydroksid blir omdannet til kalsiumkarbonat. Forskjellig fra sementmørtel som herder i reaksjon med vann.
Karbondioksid fra gjødselindustrien
I Haber-Bosch-metoden i gjødselproduksjon brukes metan (CH4) for å lage hydrogen (H2) og i prosessen blir det dannet CO2 som et biprodukt.
CH4 + H2O → CO + 3H2
CH4 + 2H2O → CO2 + 4H2
I 2018 var fler gjødselfabriker stengt, og det ble mangel på CO2 brukt i produksjon av øl og mineralvann, samt mangel på CO2 brukt i vannrenseanlegg. Vannrensing med CO2 for å gi utfelling av partikulært materiale er basert på prinsippet diffusioforese, siden H+ diffunderer raskere i vann enn HCO3- er det mulig å lage en diffusjonsgradient.
Ferrosilisiumindustri og CO2
I omdanning av jernmalm ((Fe2O3) til råjern (Fe) eller stål blir det produsert CO2. Det samme skjer når kvarts (SiO2) blir omdannet til silisium(Si) og aluminiumoksid (Al2O3) omdannet til metallisk aluminium, oksygen blir fjernet som CO2.
Reduksjoner og oksidasjoner skjer alltid i par, redokspar. En reduksjon vil si å motta elektroner eller avgi oksygen (O), mens en oksidasjon vil si å avgi elktroner eller motta oksygen (O). Al3+, Fe3+, Si4+ blir redusert fra ioneform til metall ved å motta elektroner og karbon ( C) blir oksidert til CO2 ved å motta oksygen (O).
Söderbergelektroden er en selvbrennende kontinuerlig anode brukt i elektrolyse i smelteovner for ferrosilisium, kobber eller aluminium. Den er en karbonelektrode bestående av en jernhylse fylt med tyktflytende tjære, tilsatt bitumen og kul. Det erriller på innsiden av jernhylsen som hindrer at anodematerielt renner ut når metallrøret utvider seg i varmen fra smelteprosessen.
Jernmalm, koks (karbon) og kalkstein møtes en blest (blåst) med varm luft og som gir råjern med høyt innhold av karbon. Høyt innehold av karbon gjør jernet sprøtt. Tilførsel av oksygen i en ovn fjerner karbon som CO2.
Reduksjon av hematitt (Fe2O3) til jern (Fe) med karbon (C) som blir oksidert:
2Fe2O3 + 3C → 4Fe + 3CO2
Fe2O3 + 3CO → 2Fe + 3CO2
2C + O2 → 2CO
Karbondioksid fra fermentering
Når gjær fermenterer sukker i produksjon av vin, øl, eller bakeverk blir det produsert CO2 og etanol(C2H5OH). CO2 fanget i et nettverk av glutenproteiner gir heving av bakeverk.
C6H12O6 → 2CO2 + 2 C2H5OH
Enzymet pyruvat dekarboksylase deltar i anaerob oksidasjon i etanolgjæringen og produserer CO2 og acetaldehyd. Ved fermentering blir organiske molekylder brukt som elektronakseptor i stedet for O2 som i aerob respirasjon
pyrvuat → acetaldehyd + CO2
CO2 fra vegetasjonsbrann
Grunnet klimaendringer har det de siste årene blitt stadig flere vegetasjonsbranner på Jorden hvor det blir produsert CO, CO2, nitrogenoksider og store mengder sotpartikler og svevestøv. Det kan ta lang tid før nedbrent vegetasjon igjen kan virke som en netto assimilator for CO2.
Sodavann
Kullsyreholdig vann er karbondioksid løst i vann ved høyt trykk, enten i form av rent vann med noen oppløste salter, eller som en del av innholdet i brus. Når flasken åpnes reduseres trykket og karbondioksid bruser ut i form av bobler. Jfr. Henrys lov.
Vann med oppløst karbondioksid i en karbonatisering ble oppdaget av Joseph Priestly som I 1772 skrev i «Impregnating water with fixed air; In order to communicate to the peculiar Spirit and Virtues of Pyrmont Water, And other Mineral Waters of a familiar Nature» med oppskrift for hvordan det skulle gjøres.
Priestly studerte også effekten av oksygen, oksygen oppdaget av Antoine Lavoisier og Carl Wilhelm Scheele.
Johann Jacob Schweppe (1740-1821) var en tysk-sveitsisk urmaker som utviklet et praktisk prosess for å lage karbonert mineralvann på glassflasker solgt gjennom firmaet Schweppes Company som han grunnla. Selters var et tysk varemerke fra området Selters i Hesse ved fjellkjeden Taunus. I USA brukes betegnelsen Seltzer eller Club Soda. Tonic-water er karbonert vann tilsatt kinin som smaker bittert, smakstilsatt med sitron eller lime i form av bitter lemon eller bitter lime. Sodablandevann til cocktails.
Hvis man åpner en flaske med kullsyreholdig drikke så er CO2 i starten oppløst i drikken, og helles det opp i et glass frigis CO2 fra væsken i form av gassbobler. Boblene dannes også nede i glasset ved nukleasjonspunkter ved urenheter i glasset som induserer start på boblene. og man kan noen ganger observere at boblene kommer på en linje fra ett nukleasjonspunkt.
Vulkansk aktivitet og CO2
Vulkanutbrudd gir store utslipp av CO2, SO2, vanndamp og sotpartikler i aerosoler forklart ved platetektonikk. Vulkansk aske kan spre seg i atmosfæren gir rødfargete solnedganger og reduserer solinnstråling og reduserer temperaturøkning, mens CO2 bidrar til å øke temperaturen.
Fasediagram
Fasediagram for CO2 kan finnes i fasetilstander som gass, væske eller fast form (tørris) avhengig av trykk og temperatur. I gassfase er det langt mellom CO2-molekylene og det er liten tiltrekning mellom dem. Senkes temperaturen og trykket øker kan CO2 blir omdannet til væske. Ved ennå økende trykk og lavere temperatur går CO2 over i fast form. Ved kritisk punkt-tørking av prøver analysert i transmisjonselektronmikroskop kan man under prøveopparbeidelsen erstatte den flytende fikseringsvæske med CO2 og få tørre prøver. Trippelpunkt i fasedigrammet for CO2 er -56.56°C og 4.17 bar.
Parisavtalen og klimagassutslipp
Parisavtalen er en juridisk bindende internasjonal avtale, ratifisert av Norge i 2016, som forplikter landene til å sørge for at temperaturen på Jorden ikke må overstige 2oC , helst ikke mer enn 1.5oC, og krav om klimanøytralitet innen år 2100. Klimanøytralitet vil si at utslippene er like store som opptakene. Alle land må ha en nasjonal plan for utklippskutt av klimagasser. Parisavtalen setter Norge som gasse og oljeprodusent i en klemme, og norske borgere har ikke tatt helt inn over seg hvilke endringer i vår måte å leve på som må gjøres for å oppfylle avtaleforpliktelsene.
I 2020 var de største utslippene av fossilt CO2 Kina (31%), USA (14%), EU (7%), India (7%) til sammen 59% av alle utslipp, resten av verden 41%.
Kalsiumkarbonat
Knollekalk består av hvitaktige kalksteinsknoller omgitt av mørkere skifer og er utbredt i kambro-silur-aveleiringer i Oslofeltet blant annet fra Ordovicium. Dannet fra avsetning av kalkslam og leirslam eller ved sammenpressing (konkdresjon). Kalk er lys, mens skifer er mørk.
Kalktuffer er utfelling av kalk , porøs tkalsiumkarbonat (CaCO3) med gulbrunfarge fra jernutfellinger) fra kalkrikt grunnvann som kommer opp til jordoverflaten.
Marmor (gr. marmaros –skinnende stein) er metamorf kalsiumkarbonat (kalsitt) anvendt i skulpturer og som bygningsstein utendørs og innendørs (marmormosaikk). En dråpre syre på marmos gir brusing og frigivelse av CO2.
Grunn til bekymring
Fossilt brennstoff er en viktig energibærer, og inneholder kjemiske stoffer med stor nytteeffekt. Derfor hadde det vært fornuftig på lang sikt å begrense bruk og utvinning slik at energibæreren også kunne vært tilgjengelig for seinere generasjoner. Fossilt brensel er et resultat av fotosyntesen gjennom mange hundre millioner år, og store deler av det fossilte brennstoffet blir nå omsatt til energi, karbondioksid og vann.
Når CO2-konsentrasjonen stiger i atmosfæren viser dette at det skjer endringer i de store fluksene av karbondioksid mellom hav, land og atmosfære. Spesielt gjelder dette fjerning av skog og vegetasjon, med formål brukt til beite og landbruk, industri, veibygging, hytte- og bolibygging. Fjerning av flere sjikt med vegetasjon gir redusert fotosyntese og økt respirasjon fra rotbiomasse. I tillegg ødelegges leveområder for natrulig vegetasjon, sopp og dyr, og gir minsket biodiversitet.
Karbondioksid er en av flere gasser i atmosfæren som absorberer varmestråling og bidrar til drivhuseffekten. og påvirker således Jordens klima. Det er grunn til bekymring for konsekvensene av økt konsentrasjon av CO2 og andre klimagasser i atmosfæren, habitatfragmentering og forsuringsprosesser i meget kompleks interaksjon med vann, nitrogen, svovel, fosfor og jern.
Oppdagelsen av CO2
Den nederlandske kjemikeren Jan Baptiste von Helmont fant omkring 1640 at da han brant kull hadde asken mindre masse enn det opprinnelige kullet, og det som var forsvunnet var en usynlig gas sylvestre (Historien om plantefysiologi). Den skotske kjemikeren Joseph Black oppdaget midten på 1700-tallet "fiksert luft" (karbondoksid), som var tyngre enn luft, ved å varme opp kalkstein (kalsiumkarbonat, CaCO3)) og tilsetning av syre. Ble gassen boblet gjennom en løsning av kalsiumhydroksid (Ca(OH)2) så ble det dannet utfelling av kalsiumkarbonat. Joseph Priestley beskrev i Impregnating Water with Fixed Air at det ble dannet "fiksert luft" ved å dryppe syre på kritt eller marmor, og at den fikserte luften kunne bli løst i vann.
umphry Davy og Michael Faraday klarte i 1823 å omdanne gassen CO2 til flytende form ved høyt trykk, det er overgang mellom CO2- tilstandsformene gass, væske og fast form Tørris er CO2 i fast form. ved å åpne en trykkbeholder med CO2 fant franskmannen Adrien Jean Pierre Thilorier i 1835 at det kom ut en hvitaktig "snø" ut fra flasken (tørris).

Brenning av organisk materiale produserer karbondioksid, branngasser og sotpartikler.
Litteratur
Wikipedia